解答题-实验探究题 适中0.65 引用1 组卷236
硼泥主要由MgO和SiO2组成,含有少量Fe2O3、FeO、Al2O3等杂质。用硼泥生产氢氧化镁的工艺流程如下图所示:

已知某些氢氧化物沉淀的pH如下表所示:
(1)MgO的电子式为_____ ,加入H2O2的目的是____ 。
(2)滤渣2的主要成分是_____ ,向滤渣2中继续加入过量的NaOH溶液,发生反应的离子方程式为____ 。
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为____ 。
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为____ 。
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为_______ (用含有a、b的代数式表示)。

已知某些氢氧化物沉淀的pH如下表所示:
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Al(OH)3 | 4.1 | 5.4 |
| Fe(OH)3 | 2.7 | 3.7 |
(2)滤渣2的主要成分是
(3)加入NaOH调节溶液pH=12.0时,发生反应的离子方程式为
(4)利用Mg(OH)2与含SO2的烟气反应生成MgSO4,可以使烟气脱硫,该反应的化学方程式为
(5)若取a吨硼泥为原料,最后得到b吨Mg(OH)2产品(假设生产过程中镁元素无损失),则硼泥中MgO的质量分数为
2016·贵州遵义·一模
类题推荐
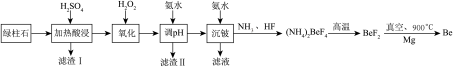
工业上常用绿柱石(主要成分3BeO•Al2O3•6SiO2,还含有铁元素)冶炼铍,其简化的工艺流程如图所示:
已知:Be和Al性质相似:几种金属阳离子的氢氧化物沉淀时的pH如表:
回答下列问题:
(1)滤渣Ⅰ的主要成分是______ ,加入H2O2的作用是______ 。
(2)得到滤渣Ⅱ的合理pH范围是______ 。
(3)用化学方程式解释不宜使用NaOH溶液来沉铍的原因是______ 。
(4)得到(NH4)2BeF4的化学方程式为______ 。
(5)由Mg还原BeF2得到Be需要真空的环境,其原因是______ 。
(6)若绿柱石中BeO的含量为a%,1吨绿柱石能生产含铍2%的合金b吨,则Be的利用率为______ 。(用含a、b的表达式表示)

已知:Be和Al性质相似:几种金属阳离子的氢氧化物沉淀时的pH如表:
| Be2+ | Al3+ | Fe3+ | Fe2+ | |
| 开始沉淀时 | 5.2 | 3.3 | 1.5 | 6.5 |
| 沉淀完全时 | 8.8 | 5.0 | 3.7 | 9.7 |
(1)滤渣Ⅰ的主要成分是
(2)得到滤渣Ⅱ的合理pH范围是
(3)用化学方程式解释不宜使用NaOH溶液来沉铍的原因是
(4)得到(NH4)2BeF4的化学方程式为
(5)由Mg还原BeF2得到Be需要真空的环境,其原因是
(6)若绿柱石中BeO的含量为a%,1吨绿柱石能生产含铍2%的合金b吨,则Be的利用率为
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
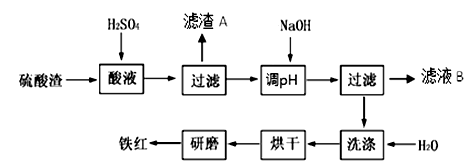
(1)硫酸渣的成分中属于两性氧化物的是______ , 写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式:______ ;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是______ ;(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
(3)滤渣A的主要成分为______ ,滤液B可以回收的物质有Na2SO4、MgSO4和______ ;
(4)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为______ (用最简分数表达式表示)。

(1)硫酸渣的成分中属于两性氧化物的是
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(4)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



