解答题-原理综合题 适中0.65 引用2 组卷1098
请回答下列问题:
(1)纯水在T ℃时pH=6,该温度下1 mol/L的NaOH溶液中,由水电离出的c(OH-)=_______ mol/L。
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A)__________ pH(B) (填“>”、“=”或“<”);现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)_________ V(B)(填“>”、“=”或“<”)。
(3)已知:二元酸H2R 的电离方程式是: ,
, ,若0.1mol•L﹣1NaHR溶液的c(H+)="a"
,若0.1mol•L﹣1NaHR溶液的c(H+)="a"  ,则0.1
,则0.1  H2R溶液中c(H+)
H2R溶液中c(H+)___________ (0.1+a)  (填“<”、“>”或“=”),理由是
(填“<”、“>”或“=”),理由是______________ 。
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
①25 ℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为________ (用化学式表示)。
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为__________________ 。
(1)纯水在T ℃时pH=6,该温度下1 mol/L的NaOH溶液中,由水电离出的c(OH-)=
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A)
(3)已知:二元酸H2R 的电离方程式是:
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K= |
| CH3COOH[] | K= |
| H2CO3 | K1= |
①25 ℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
16-17高二上·天津·期中
类题推荐
水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在 100℃时,pH=6,该温度下 0.1mol•L﹣1 的 NaOH 溶液中,溶液的 pH=_____ 。
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为_____ , 由水电离出的 c(OH﹣)=_____ mol•L﹣1。
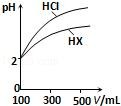
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是_____ (填“强酸”或“弱酸”),理由是_____ 。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为________ (填化学式)。
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的_________ 倍。
(1)纯水在 100℃时,pH=6,该温度下 0.1mol•L﹣1 的 NaOH 溶液中,溶液的 pH=
(2)25℃时,向水中加入少量碳酸钠固体,得到 pH 为 11 的溶液,其水解的离子方程式为
(3)体积均为 100mL、pH 均为 2 的盐酸与一元酸 HX,加水稀释过程中 pH 与溶液体积的关系如图所示,则 HX 是

(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10﹣10 |
| CH3COOH | K=1.8×10﹣5 |
| H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
①25℃时,等浓度的 NaCN 溶液、Na2CO3 溶液和 CH3COONa 溶液,pH 由大到小的顺序为
②25℃时,在 0.5mol/L 的醋酸溶液中由醋酸电离出的 c(H+)约是由水电离出的 c(H+)的
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 R2﹣+H+,
R2﹣+H+,

