单选题 适中0.65 引用6 组卷1002
已知热化学方程式:
H2O(g)=H2(g)+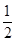 O2(g) ΔH=+241.8 kJ/mol
O2(g) ΔH=+241.8 kJ/mol
H2(g)+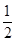 O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )
O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )
H2O(g)=H2(g)+
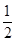 O2(g) ΔH=+241.8 kJ/mol
O2(g) ΔH=+241.8 kJ/molH2(g)+
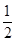 O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )
O2(g)=H2O(l) ΔH=-285.8 kJ/mol,当1 g液态水变为水蒸气时,其热量变化是( )| A.ΔH=+88 kJ/mol | B.ΔH=+2.44 kJ/mol |
| C.ΔH=-4.98 kJ/mol | D.ΔH=-44 kJ/mol |
2016高二·全国·课时练习
类题推荐
已知在1.01×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
| A.2H2(g)+O2(g)=2H2O(l) ΔH=-484 kJ·mol-1 |
B.H2O(g)=H2(g)+ O2(g) ΔH=+242 kJ·mol-1 O2(g) ΔH=+242 kJ·mol-1 |
C.H2(g)+ O2(g)=H2O(g) ΔH=-484kJ·mol-1 O2(g)=H2O(g) ΔH=-484kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g) ΔH=+484 kJ·mol-1 |
已知H—H键的键能为436 kJ/mol,O=O键的键能为498 kJ/mol,根据热化学方程式H2(g)+ O2(g)=H2O(l) ΔH=-286 kJ/mol,判断H2O分子中O—H键的键能为
O2(g)=H2O(l) ΔH=-286 kJ/mol,判断H2O分子中O—H键的键能为
| A.485.5 kJ/mol | B.610 kJ/mol |
| C.917 kJ/mol | D.1 220 kJ/mol |
已知:H2(g)+1/2O2(g)=H2O(l) ΔH1=-285.8 kJ·mol-1 ①
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1 ②
O2(g)=O2(l) ΔH3=-6.84 kJ·mol-1 ③
H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1 ④
下列说法正确的是
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1 ②
O2(g)=O2(l) ΔH3=-6.84 kJ·mol-1 ③
H2O(g)=H2O(l) ΔH4=-44 kJ·mol-1 ④
下列说法正确的是
| A.上述四个反应都是吸热反应 |
| B.1 mol液态H2的能量大于1 mol气态H2的能量 |
| C.H2的燃烧热ΔH为-285.8 kJ·mol-1 |
| D.火箭中液氢燃烧的热化学方程式为H2(l)+1/2O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


