解答题-实验探究题 容易0.94 引用1 组卷296
NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。写出化学反应方程式:_________________________________ 。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分,从而判断该消毒液是否变质。
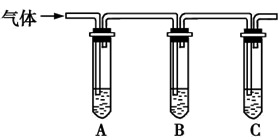
限选试剂:98%浓硫酸、1%品红溶液、1.0 mol·L-1 KI-淀粉溶液、1.0 mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
请完成下列实验方案。
(3)用滴定法测定消毒液中NaClO的浓度。实验步骤如下:
①量取 25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液b mL。
②滴定分析。将c mol·L-1的酸性KMnO4溶液装入______ (填“酸式”或“碱式”)滴定管中滴定,使KMnO4和剩余的Na2SO3发生反应。当溶液由无色变成浅红色,且半分钟内红色保持不褪去时,停止滴定,记录数据。重复滴定实验3次,测得平均消耗酸性KMnO4溶液V mL;滴定过程中涉及的反应有:NaClO+Na2SO3=NaCl+Na2SO4 ;2KMnO4+5Na2SO3+3H2SO4=K2SO4+2MnSO4+5Na2SO4+3H2O。
③计算。消毒液中NaClO的浓度为__ mol·L-1(用含a、b、c、V的代数式表示)。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO而变质。写出化学反应方程式:
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分,从而判断该消毒液是否变质。

限选试剂:98%浓硫酸、1%品红溶液、1.0 mol·L-1 KI-淀粉溶液、1.0 mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
请完成下列实验方案。
| 所加试剂 | 预期现象和结论 |
| 向试管A中加足量①; 试管B中加1%品红溶液; 试管C中加②。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质; ③ ④ |
①量取 25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液b mL。
②滴定分析。将c mol·L-1的酸性KMnO4溶液装入
③计算。消毒液中NaClO的浓度为
2016·湖南郴州·模拟预测
类题推荐
高一化学研修小组发现了一瓶消毒液(主要成分为 和
和 ),并对其展开研究:
),并对其展开研究:
已知: 和
和 在酸性条件下可发生反应:
在酸性条件下可发生反应: 。
。
(1)消毒液中的 可吸收空气中的
可吸收空气中的 生成
生成 和
和 。写出反应的化学方程式
。写出反应的化学方程式__________________ 。而后 分解,使消毒液变质失效。
分解,使消毒液变质失效。
(2)取适量消毒液于试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
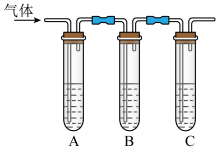
限选试剂: 浓硫酸、
浓硫酸、 品红溶液(遇漂白性物质红色褪去)、
品红溶液(遇漂白性物质红色褪去)、 溶液(含淀粉)、
溶液(含淀粉)、
 溶液、澄清石灰水、饱和
溶液、澄清石灰水、饱和 溶液、
溶液、 溶液。
溶液。
请完成下列实验方案。
(3)商业上常用“有效氯”来说明消毒剂的消毒能力。“有效氯”指一定质量的消毒剂与多少质量的氯气氧化能力相当,该数值以消毒剂中氯气的质量分数来表示。例如, 某消毒液与
某消毒液与 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是 。研修小组的同学们对该瓶消毒液的“有效氯”含量进行了测定,实验步骤如下:
。研修小组的同学们对该瓶消毒液的“有效氯”含量进行了测定,实验步骤如下:
①取 消毒液放入锥形瓶中,加入过量的
消毒液放入锥形瓶中,加入过量的 溶液
溶液 ;
;
②定量测定:向锥形瓶中滴加 的酸性
的酸性 溶液,使之和剩余的
溶液,使之和剩余的 溶液反应,恰好完全反应时,消耗
溶液反应,恰好完全反应时,消耗 溶液
溶液 。
。
测定过程中涉及的反应有: ;
;

该消毒液的“有效氯”含量为____________________ 。(用含a、b、c、V的代数式表示)。
已知:
(1)消毒液中的
(2)取适量消毒液于试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。

限选试剂:
请完成下列实验方案。
所加试剂 | 预期现象和结论 |
| 试管A中加① 试管B中加② 试管C中加澄清石灰水。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊。则消毒液部分变质; 若③ |
(3)商业上常用“有效氯”来说明消毒剂的消毒能力。“有效氯”指一定质量的消毒剂与多少质量的氯气氧化能力相当,该数值以消毒剂中氯气的质量分数来表示。例如,
①取
②定量测定:向锥形瓶中滴加
测定过程中涉及的反应有:
该消毒液的“有效氯”含量为
某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl- + 2H+ = Cl2↑+ H2O。某学习小组拟探究该消毒液的变质情况。
(1)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过下列装置检验气体的成分可以判断消毒液是否变质。
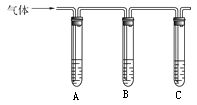
学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙:______ 。
为了验证可能为甲,请完成下列实验方案。限选试剂:
a.98%的浓硫酸 b.1%的品红溶液 c.1.0 mol·L-1的KI-淀粉溶液
d.1.0 mol·L-1 的NaOH溶液 e.澄清石灰水 f.饱和NaCl溶液
(2)用滴定法测定消毒液中NaClO的浓度。
①在使用滴定管之前首先进行的操作是_____________________ ;
②量取25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液v1 mL;(反应的化学方程式为:NaClO + Na2SO3 = NaCl+ Na2SO4)将b mol·L-1的用硫酸酸化的KMnO4溶液装入_________ (填仪器名称)中;滴定剩余的Na2SO3溶液,反应的化学方程式为:_______________ 。当溶液由__________ (填滴定终点现象)停止滴定,记录数据。
③重复上述滴定操作2次,平均消耗酸性KMnO4溶液v2 mL。则消毒液中NaClO的浓度为_______ mol·L-1(用含a、b、v1、v2的代数式表示)。
(1)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过下列装置检验气体的成分可以判断消毒液是否变质。

学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙:
为了验证可能为甲,请完成下列实验方案。限选试剂:
a.98%的浓硫酸 b.1%的品红溶液 c.1.0 mol·L-1的KI-淀粉溶液
d.1.0 mol·L-1 的NaOH溶液 e.澄清石灰水 f.饱和NaCl溶液
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量 试管B中加1%品红溶液; 试管C中加 | 若A中 B中 C中 |
①在使用滴定管之前首先进行的操作是
②量取25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液v1 mL;(反应的化学方程式为:NaClO + Na2SO3 = NaCl+ Na2SO4)将b mol·L-1的用硫酸酸化的KMnO4溶液装入
③重复上述滴定操作2次,平均消耗酸性KMnO4溶液v2 mL。则消毒液中NaClO的浓度为
NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO。写出化学反应方程式___ 。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
限选试剂:98%浓硫酸、1%品红溶液、1.0mol·L-1KI淀粉溶液、1.0mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。

请完成下列实验方案。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO。写出化学反应方程式
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
限选试剂:98%浓硫酸、1%品红溶液、1.0mol·L-1KI淀粉溶液、1.0mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。

请完成下列实验方案。
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量① 试管B中加1%品红溶液; 试管C中加② | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质;③ |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


