单选题 适中0.65 引用2 组卷662
常温下,用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L HCl溶液,滴定曲线,如图所示,下列说法不正确的是
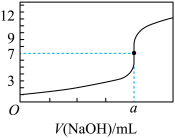

| A.a=20.00 |
| B.滴定过程中,可能存在: |
| C.若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D.若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00 |
11-12高三上·北京朝阳·期末
类题推荐
常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L的盐酸和醋酸溶液,滴定过程中溶液pH的变化曲线如图所示。下列说法中,正确的是
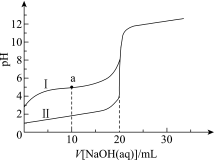
| A.曲线I表示滴定盐酸 |
| B.a点浓度最大的离子是Na+ |
| C.V[NaOH(aq)]=20 mL时,c(Cl−)=c(CH3COO−) |
| D.用酚酞作指示剂,达到滴定终点时,溶液从无色刚好变为粉红色,且半分钟内不变色 |
常温下,用0.1000 mol/L NaOH溶液滴定20.00 mL 0.1000 mol/L  溶液所得滴定曲线如图,下列说法正确的是
溶液所得滴定曲线如图,下列说法正确的是


| A.常温下,水的电离程度:④>③>② |
| B.②点时, |
| C.由②到③点过程中 |
| D.④点时, |
常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL0.1000 mol/L醋酸溶液,得到2条滴定曲线,如图所示。若用HA表示酸,下列说法正确的是
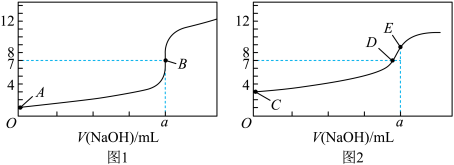

| A.滴定盐酸的曲线是图2 |
| B.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A﹣) |
| C.达到B、E状态时,反应消耗的n(CH3COOH)=n(HCl) |
| D.当V(NaOH)=20.00 mL时,两混合溶液中各离子浓度由大到小的顺序均为c(Na+)>c(A﹣)>c(OH﹣)>c(H+) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


