单选题 适中0.65 引用1 组卷171
已知:NaA的水溶液呈碱性。常温下将等体积的0.10 mol·L-1NaA溶液与0.05 mol·L-1 HCl溶液混合,所得溶液pH<7。据此判断以下说法不成立的是
| A.c(Cl-)+c(OH-)+c(A-)>c(Na+) | B.相同条件下HA的电离程度大于A-的水解程度 |
| C.c(A-)+ c(HA)= c(Na+) | D.c(A-)>c(Na+) >c(H+)>c(OH-) |
2016·宁夏银川·三模
类题推荐
常温下,0.1 mol·L-1的一元酸HA与0.1 mol·L-1的NaOH溶液等体积混合后,所得溶液pH>7,下列说法正确的是
| A.混合前一元酸HA的c(H+)=0.1 mol·L-1 |
| B.该混合溶液中:c(Na+)>c(A-)>c(OH-)>c(H+) |
| C.HA在水溶液中的电离方程式:HA = H+ + A- |
| D.该混合溶液中:c(A-)+ c(HA)=0.1 mol·L-1 |
室温条件下,用0.100 mol·L-1的NaOH溶液分别滴定HA和HB两种酸溶液,两种酸溶液的体积均为20.00 mL,浓度均为0.100 mol·L-1,滴定曲线如图所示。下列叙述正确的是


| A.HA可以是醋酸,HB可以是HCl |
| B.浓度相等时,B-的水解程度大于HB的电离程度 |
| C.V(NaOH)=20.00 mL时,c(Na+)=c(A-)>c(B-) |
| D.pH=7时,滴定HB溶液消耗的V(NaOH)>20.00 mL |
常温下,现有浓度都为0.1mol·L-1HA、HB的溶液各20mL,分别用0.1 mol·L-1NaOH溶液滴定。溶液的pH与加入NaOH溶液体积V的关系如图所示。下列判断错误的是
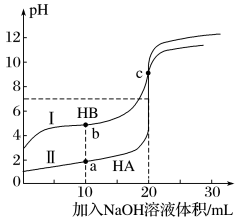

| A.滴定过程中,水电离的c(H+)·c(OH-)均不变 |
| B.相同条件下,HB的电离程度小于HA的电离程度 |
| C.V=10mL时,c(HB)+c(B-)=2c(Na+) |
| D.V=20mL时,c(A-)>c(B-) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


