填空题 适中0.65 引用2 组卷943
超重元素的假设预言自然界中可能存在114号的稳定同位素X,请根据原子结构理论和元素周期律预测:
(1)X元素位于周期表中第____ 周期,_____ 族,为_____ 元素(金属或非金属)
(2)写出其最高价氧化物及其水化物的化学式分别为___________ 、__________ ,并估计后者为________ 性(填“酸”或“碱”)
(1)X元素位于周期表中第
(2)写出其最高价氧化物及其水化物的化学式分别为
9-10高一下·西藏拉萨·期末
类题推荐
如表为10种元素在元素周期表中的位置,请回答有关问题:
(1)⑥和⑨形成的化合物为_______ (填离子或共价)化合物,电子式为_______ 。
(2)表中最活泼的金属是_______ (填元素符号,下同),非金属性最强的元素是_______ 。
(3)表中能形成两性氢氧化物的元素是_______ ,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物对应的水化物反应的化学方程式:_______ 、_______ 。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:_______ 。
| ⅠA | ⅡA | … | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(1)⑥和⑨形成的化合物为
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年,元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
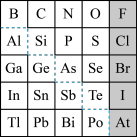
(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4___ H2SeO4(填“>”、“<”或“=”)。
②氢化物的还原性:H2O___ H2S(填“>”、“<”或“=”)。
(2)可在图中分界线(虚线部分)附近寻找___ (填序号)。
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为___ 。
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是___ (填字母)。
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。

(1)根据元素周期律,推断:
①H3AsO4、H2SeO4的酸性强弱:H3AsO4
②氢化物的还原性:H2O
(2)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂B.半导体材料C.合金材料D.农药
(3)①Se2Cl2常用作分析试剂,其电子式为
②硒(Se)化铟(In)是一种可应用于未来超算设备的新型半导体材料。下列说法正确的是
A.原子半径:In>Se B.In的金属性比Se强
C.In的金属性比Al弱 D.硒化铟的化学式为InSe2
(4)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)。
| 实验步骤 | 实验现象与结论 |
| 在试管中加入 | 现象: |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



