解答题-工业流程题 适中0.65 引用4 组卷554
过氧化钙(CaO2)难溶于水,在常温下稳定,在潮湿空气及水中缓慢分解放出氧气,因而广泛应用于渔业、农业、环保等许多方面。下图是以大理石(主要杂质是氧化铁)等为原料制取过氧化钙(CaO2)的流程。
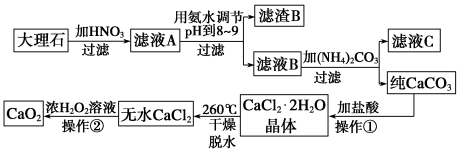
请回答下列问题:
(1)操作①应包括下列操作中的____________ 。(填序号)
A.溶解 B.过滤 C.蒸馏 D.分液 E.蒸发结晶
(2)用氨水调节pH至8~9的目的是_________________________________ 。
(3)若测得滤液c中c(CO32-)=10-3mol/L,则Ca2+____ (填“是”或“不”)沉淀完全。[已知c(Ca2+)≤10-5 mol/L时即可视为沉淀完全;Ksp(CaCO3)=4.96×10-9]
(4)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中c(NH4+)_______ c(NO3-)(填“≥”、“≤”、“<”、“>”或“=”)。
(5)操作②是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9~11,才出现大量沉淀。写出该反应的化学方程式_________________________ ;用简要的文字解释用氢氧化钠调节pH至9~11的原因____________ 。
(6)已知大理石含CaCO3的质量分数为a,m g大理石可以制得n g CaO2,请计算:CaCO3转化为CaO2过程中,Ca原子的利用率__________________ 。

请回答下列问题:
(1)操作①应包括下列操作中的
A.溶解 B.过滤 C.蒸馏 D.分液 E.蒸发结晶
(2)用氨水调节pH至8~9的目的是
(3)若测得滤液c中c(CO32-)=10-3mol/L,则Ca2+
(4)若在滤液C中,加入HNO3使溶液呈酸性以得到副产物NH4NO3,则酸化后溶液中c(NH4+)
(5)操作②是:在低温下,往过氧化氢浓溶液中投入无水氯化钙进行反应,一段时间后,再加入氢氧化钠溶液,当调节溶液pH至9~11,才出现大量沉淀。写出该反应的化学方程式
(6)已知大理石含CaCO3的质量分数为a,m g大理石可以制得n g CaO2,请计算:CaCO3转化为CaO2过程中,Ca原子的利用率
2010·福建泉州·一模
类题推荐
铍及其化合物用途广泛,以绿柱石(主要组成是3BeO·Al2O3·6SiO2, 还含少量铁元素)和方解石(主要成分是CaCO3)为原料生产铍的工艺流程如图所示:

已知:①铝铵矾[NH4Al(SO4 )2·12H2O]在不同温度下的溶解度如下表:
②Be(OH)2性质和Al(OH)3相似,是两性氢氧化物。
回答下列问题:
(1)绿柱石中Be的化合价为___________ 。“熔炼”中生成气体的电子式为 ___________ 。
(2)滤渣1中除SiO2及难溶性硅酸盐外,还含有___________ (填化学式); “转化”后,要得到铝铵矾晶体,在中学实验室中可采取的操作是___________ 、___________ 、过滤、 洗涤、干燥。
(3)加H2O2时,溶液中发生反应的离子方程式是___________ 。
(4)“沉铍”时,若选用氢氧化钠溶液可能造成的影响是___________ ,所得母液中的主要溶质可返回到___________ 工序循环利用。
(5)“沉铍”时加入氨水调节pH至7.5,列式并计算说明此时溶液中的铍离子是否沉淀完全___________ 。(已知:该条件下,Ksp[Be(OH)2]=1.6×10-22; 离子浓度≤1×10-5mol·L-1时,可认为离子沉淀完全。)

已知:①铝铵矾[NH4Al(SO4 )2·12H2O]在不同温度下的溶解度如下表:
| 温度/°C | 0 | 10 | 20 | 30 | 40 | 60 |
| 溶解度/g | 2.10 | 5.00 | 7.74 | 10.9 | 14.9 | 26.7 |
回答下列问题:
(1)绿柱石中Be的化合价为
(2)滤渣1中除SiO2及难溶性硅酸盐外,还含有
(3)加H2O2时,溶液中发生反应的离子方程式是
(4)“沉铍”时,若选用氢氧化钠溶液可能造成的影响是
(5)“沉铍”时加入氨水调节pH至7.5,列式并计算说明此时溶液中的铍离子是否沉淀完全
工业上常用辉铜矿(主要成分为Cu2S,含有Fe2O3、CaO、SiO2等杂质)制备重要催化剂CuCl。工艺如下:

已知:①CuCl为难溶于水的白色固体
②部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
请回答下列问题:
(1)“浸取”过程中Cu2S转化为可溶性铜盐的离子方程式为:___________ 。
(2)“浸取“是该工艺的第一步,提高浸出率可提高最终产品产率。工程师研究发现单独加入FeCl3溶液时Cu2+浸出率很低,但同时加入FeCl3溶液和H2O2时可提高Cu2+浸出率,写出H2O2与Fe2+反应的离子方程式___________ 。进一步研究发现,加入H2O2后随温度升高,一定时间后Cu2+浸出率随温度变化的曲线如图。请分析温度高于85℃,Cu2+浸出率下降的原因___________ 。

(3)已知Ksp(CaF2)=4.0×10−11经测定“浸出液”中Ca2+浓度为4.0×10−3mol·L−1,加入NaF除去溶液中Ca2+,当溶液中c(F-)=1.0×10−3mol·L−1时,溶液中Ca2+浓度为___________ mg/L。
(4)“除铁”过程包括氧化Fe2+、加入CuO调节pH等过程,为达到“除铁”目的需调节溶液pH范围为___________ 。
(5)“还原”过程中反应的离子方程式为:___________ 。
(6)通过“操作X”为过滤 ,___________ ,___________ (填操作名称),最终得到CuCl产品。

已知:①CuCl为难溶于水的白色固体
②部分金属阳离子生成氢氧化物沉淀的pH范围如下表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Cu2+ | 4.4 | 6.4 |
(1)“浸取”过程中Cu2S转化为可溶性铜盐的离子方程式为:
(2)“浸取“是该工艺的第一步,提高浸出率可提高最终产品产率。工程师研究发现单独加入FeCl3溶液时Cu2+浸出率很低,但同时加入FeCl3溶液和H2O2时可提高Cu2+浸出率,写出H2O2与Fe2+反应的离子方程式

(3)已知Ksp(CaF2)=4.0×10−11经测定“浸出液”中Ca2+浓度为4.0×10−3mol·L−1,加入NaF除去溶液中Ca2+,当溶液中c(F-)=1.0×10−3mol·L−1时,溶液中Ca2+浓度为
(4)“除铁”过程包括氧化Fe2+、加入CuO调节pH等过程,为达到“除铁”目的需调节溶液pH范围为
(5)“还原”过程中反应的离子方程式为:
(6)通过“操作X”为过滤 ,
以某铁钴矿(主要成分为 FeCo2S4,还含有少量 MgO、SiO2等杂质)为原料制取金属钴和黄钠铁矾的工艺流程如图所示:
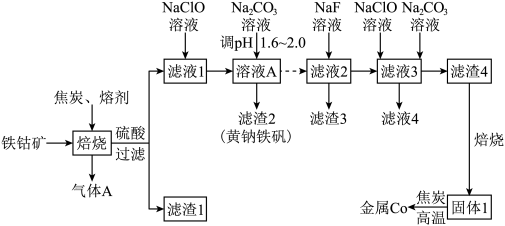
可能用到的常数:
请回答下列问题:
(1)焙烧铁钴矿时,产生气体A 的主要成分有_______ ;滤渣 1 的主要成分为_______ 。
(2)在溶液A中加入适量的Na2CO3调节pH 为 1.6~2.0,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式_______ ,此步骤加入Na2CO3不宜过量,原因是_______ 。
(3)确定滤液1中的Fe2+已被氧化完全的方法_______ 。
(4)已知:当离子浓度小于 1.0×10−5mol/L 时,可认为沉淀完全。25℃时,在滤液 2 中加入NaF溶液,当溶液中 Mg2+刚好沉淀完全时,测得溶液的pH为3.5,此时溶液中HF的浓度为_______ mol/L。
(5)流程中NaClO溶液和 Na2CO3溶液必须分两次依次加入,请解释原因_______ 。
(6)经检测,滤渣4是由 Co(OH)3和Co(OH)SO4形成的混合物,请写出后者焙烧时发生的化学反应方程式_______ 。

可能用到的常数:
| 溶度积 Ksp | 电离平衡常数 Ka | |||||
| MgF2 | Mg(OH)2 | Co(OH)2 | Fe(OH)2 | Fe(OH)3 | Co(OH)3 | HF |
| 6.4×10−9 | 1.8×10−11 | 1.6×10−15 | 8.0×10−16 | 4.0×10−38 | 1.6×10−44 | 3.6×10−4 |
(1)焙烧铁钴矿时,产生气体A 的主要成分有
(2)在溶液A中加入适量的Na2CO3调节pH 为 1.6~2.0,生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式
(3)确定滤液1中的Fe2+已被氧化完全的方法
(4)已知:当离子浓度小于 1.0×10−5mol/L 时,可认为沉淀完全。25℃时,在滤液 2 中加入NaF溶液,当溶液中 Mg2+刚好沉淀完全时,测得溶液的pH为3.5,此时溶液中HF的浓度为
(5)流程中NaClO溶液和 Na2CO3溶液必须分两次依次加入,请解释原因
(6)经检测,滤渣4是由 Co(OH)3和Co(OH)SO4形成的混合物,请写出后者焙烧时发生的化学反应方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


