解答题-原理综合题 适中0.65 引用3 组卷406
化学反应原理在科研和工农业生产中有广泛应用。
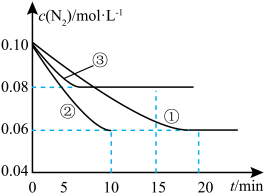
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g) 2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
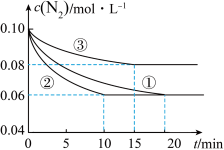
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=__________________ ;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的__________ 、__________ (填字母编号)。
a.增大压强
b.减小压强
c.升高温度
d.降低温度
e.使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g) N2O4(g)。
N2O4(g)。
①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)=0.05mol/L,则该反应的平衡常数K=__________ ;
②已知N2O4在较高温度下难以稳定存在,易转化为NO2,若升高温度,上述反应的平衡常数K将__________ (填“增大”、“减小”或“不变”)。
③向绝热密闭容器中通入一定量的NO2,某时间段内正反应速率随时间的变化如图所示。下列说法正确的是__________ (填字母编号)。
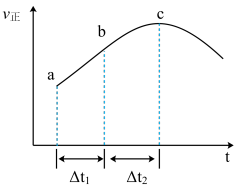
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.Δt1=Δt2时,NO2的转化率:a~b段小于 b~c段
(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,反应后溶液恰好显中性,则a______ b。 (填“>”、“<”或“=”);用a、b表示NH3 H2O的电离平衡常数Kb=
H2O的电离平衡常数Kb=________________ 。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g)

实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=
a.增大压强
b.减小压强
c.升高温度
d.降低温度
e.使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g)
①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)=0.05mol/L,则该反应的平衡常数K=
②已知N2O4在较高温度下难以稳定存在,易转化为NO2,若升高温度,上述反应的平衡常数K将
③向绝热密闭容器中通入一定量的NO2,某时间段内正反应速率随时间的变化如图所示。下列说法正确的是

A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.Δt1=Δt2时,NO2的转化率:a~b段小于 b~c段
(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,反应后溶液恰好显中性,则a
15-16高三上·山东日照·阶段练习
类题推荐
化学反应原理在科研和工农业生产中有广泛应用。
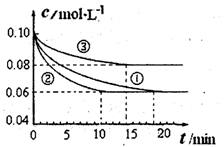
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g) 2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
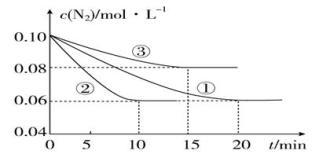
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=____________ ;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的________ 、________ (填字母编号)。
a.增大压强 b.减小压强 c.升高温度 d.降低温度 e.使用催化剂
(2)800 K时向下列起始体积相同的密闭容器中充入2 mol N2、3 mol H2,甲容器在反应过程中保持温度压强不变,乙容器保持温度体积不变,丙容器是绝热容器保持体积不变,三容器各自建立化学平衡。
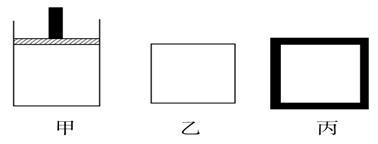
①达到平衡时,平衡常数K甲________ K乙________ K丙(填“>”“<”或“=”)。
②达到平衡时N2的浓度c(N2)甲________ c(N2)乙,c(N2)乙________ c(N2)丙(填“>”“<”或“=”)。
③对甲、乙、丙三容器的描述,以下说法正确的是____________ 。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g)
 2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
2NH3(g) ΔH<0。在1 L 密闭容器中加入0.1 mol N2和0.3 mol H2,实验①、②、③中c(N2)随时间(t)的变化如图所示:
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=
a.增大压强 b.减小压强 c.升高温度 d.降低温度 e.使用催化剂
(2)800 K时向下列起始体积相同的密闭容器中充入2 mol N2、3 mol H2,甲容器在反应过程中保持温度压强不变,乙容器保持温度体积不变,丙容器是绝热容器保持体积不变,三容器各自建立化学平衡。

①达到平衡时,平衡常数K甲
②达到平衡时N2的浓度c(N2)甲
③对甲、乙、丙三容器的描述,以下说法正确的是
| A.甲容器气体密度不再变化时,说明此反应已达到平衡状态 |
| B.在乙中充入稀有气体He,化学反应速率加快 |
| C.丙容器温度不再变化时说明已达平衡状态 |
| D.向丙容器中充入氨气,正向速率减小,逆向速率增大 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2NH3(g)
2NH3(g)