填空题 适中0.65 引用1 组卷612
下图是工业生产硝酸铵的流程。
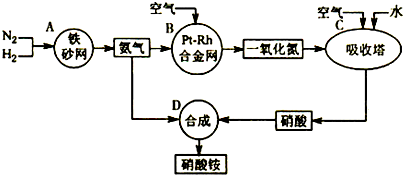
(1)吸收塔C中通入空气的目的是_________________________________ 。
A、B、C、D四个容器中的反应,属于氧化还原反应的是_______ (填字母)。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H = -1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
写出氨高温催化氧化的热化学方程式:_______ ,氨催化氧化反应的化学平衡常数表达式K=_____ 。
(3)已知:N2(g)+3H2(g) 2NH3(g) △H= -92 kJ/mol。为提高氢气的转化率,宜采取的措施有
2NH3(g) △H= -92 kJ/mol。为提高氢气的转化率,宜采取的措施有_______ 。(填字母)
A.升高温度 B.使用催化剂 C.增大压强
D.循环利用和不断补充氮气 E.及时移出氨
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,此时H2的转化率为________ 。

(1)吸收塔C中通入空气的目的是
A、B、C、D四个容器中的反应,属于氧化还原反应的是
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H = -1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H=+180.5 kJ/mol
写出氨高温催化氧化的热化学方程式:
(3)已知:N2(g)+3H2(g)
 2NH3(g) △H= -92 kJ/mol。为提高氢气的转化率,宜采取的措施有
2NH3(g) △H= -92 kJ/mol。为提高氢气的转化率,宜采取的措施有A.升高温度 B.使用催化剂 C.增大压强
D.循环利用和不断补充氮气 E.及时移出氨
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,此时H2的转化率为
9-10高二下·江苏·期末
类题推荐
(1)已知反应Ⅰ:4NH3(g)+3O2(g)==2N2(g)+6H2O(g) △H=-1266.8kJ/mol
反应Ⅱ:N2(g) + O2(g)="=" 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式________________________________ ,该反应的化学平衡常数的表达式K=___________ (用含K1、K2的代数式表示)。
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为:_______________________ 。该电池使用过程中,正极附近溶液的pH将____ (填“升高”、“降低”或“不变”)。
(2)已知:N2(g) +3H2(g) 2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。
①为提高H2的转化率,宜采取的措施有____________ (填字母)
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为________________ 。
反应Ⅱ:N2(g) + O2(g)="=" 2NO(g) △=+180.5kJ/mol
它们的平衡常数依次为K1、K2
①写出氨高温催化氧化生成NO的热化学方程式
②反应Ⅰ可设计成燃料电池,若该电池以KOH溶液作电解质溶液,则负极的电极反应式为:
(2)已知:N2(g) +3H2(g)
 2NH3(g) △H=-92kJ/mol。
2NH3(g) △H=-92kJ/mol。①为提高H2的转化率,宜采取的措施有
| A.及时移出氨 | B.升高温度 |
| C.使用催化剂 | D.循环利用和不断补充N2 |
②在一定温度、压强下,将N2和H2按体积比1:3在密闭容器中混合,当反应达平衡时,测得平衡混合气体中NH3的体积分数为25%,此时H2的转化率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网

 2NH3(g) ΔH=-92.4 kJ·mol-1。
2NH3(g) ΔH=-92.4 kJ·mol-1。
 2NH3(g)
2NH3(g)


