解答题-工业流程题 容易0.94 引用1 组卷810
(Ⅰ)混合物的分离与提纯在化学实验中占有重要的位置。下图表示从固体混合物中分离X的方案,请回答有关问题。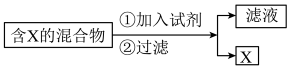
(1)若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是_______ ,有关反应的化学方程式为______________ ;
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作)__________________________ 。
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(3)该工艺的中间过程会发生反应: ,反应的氧化剂是
,反应的氧化剂是______________ ,氧化产物为__________
(4)在精炼铜的过程中,电解液中 逐渐下降,
逐渐下降, 、
、 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的 、
、 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
甲同学设计了如下除杂方案:
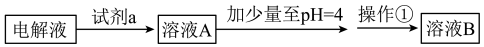
①试剂a是__________ ,其目的是____________________________________ ;根据溶度积该方案能够除去的杂质金属阳离子是____________ 。写出检验该杂质金属阳离子的操作方法:_______________________________________________ .
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使 生成
生成 沉淀而除去”,乙同学认为甲同学的方案中也
沉淀而除去”,乙同学认为甲同学的方案中也
应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________ (填“是”或“否”),理由是_________________________________________________ 。

(1)若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作)
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(3)该工艺的中间过程会发生反应:
 ,反应的氧化剂是
,反应的氧化剂是(4)在精炼铜的过程中,电解液中
| 物质 | ||||
| 溶度积 |
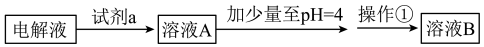
①试剂a是
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使
应该将溶液pH调至7~8。你认为乙同学的建议是否正确?
2010·四川绵阳·一模
类题推荐
通过火法治金炼出的铜是粗铜,含杂质金、银、铁、锌,不适于电器及其他许多工业使用,必须进行电解精炼。
⑴在精炼铜时,阳极减小的质量与阴极增加的质量是否相等______ (填“是”或“否”);阳极下面沉积金属的成分主要是________ 。
⑵在精炼铜的过程中,Cu2+浓度逐渐下降,c(Fe2+)、c(Zn2+)会逐渐________ ,所以需要定时除去其中的Fe2+、Zn2+。甲同学设计了下列除杂方案I(见下图)。
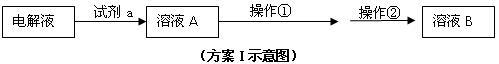
请参照下表给出的数据,回答下列问题:
①试剂a是______________ ,其目的是______________ 。
②操作①调节pH至b,b的取值范围是____________ 。
③调节溶液A的PH时可选择下列哪些试剂________ 。
A.NaOH B.CuO C.Cu(OH)2 D.NH3·H2O E.Cu2(OH)2CO3
④操作②是___________ ,方案I中不能够除去的杂质金属阳离子是_______ 。
⑶乙同学在查阅课本时发现,“工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节pH至7-8,可使Fe3+生成Fe(OH)3沉淀而除去。”乙同学认为甲同学的方案I中也应该将溶液pH调至7-8。
你认为乙同学的建议是否正确?_________ (填“是”或“否”)理由是________ 。
⑴在精炼铜时,阳极减小的质量与阴极增加的质量是否相等
⑵在精炼铜的过程中,Cu2+浓度逐渐下降,c(Fe2+)、c(Zn2+)会逐渐

请参照下表给出的数据,回答下列问题:
| 物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 | Zn(OH)2 |
| 开始沉淀时的pH | 7.6 | 5.2 | 2.7 | 8.0 |
| 完全沉淀时的pH | 9.6 | 6.7 | 3.7 | 11.0 |
①试剂a是
②操作①调节pH至b,b的取值范围是
③调节溶液A的PH时可选择下列哪些试剂
A.NaOH B.CuO C.Cu(OH)2 D.NH3·H2O E.Cu2(OH)2CO3
④操作②是
⑶乙同学在查阅课本时发现,“工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节pH至7-8,可使Fe3+生成Fe(OH)3沉淀而除去。”乙同学认为甲同学的方案I中也应该将溶液pH调至7-8。
你认为乙同学的建议是否正确?
(1)以黄铜矿冶炼金属铜的过程中发生反应:2Cu2O+Cu2S 6Cu+SO2↑,反应的氧化剂是
6Cu+SO2↑,反应的氧化剂是_____________________ 。
(2) 黄铜矿熔炼后得到的粗铜含少量Fe、Zn、Ag、Au等金属杂质,需进一步采用电解法精制。在电解精炼铜时,电解液中除了硫酸铜外,往往再加入一些硫酸,其作用是_____________________ 。
(3)在精炼铜的过程中,电解液中c(Cu2+)逐渐下降,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。下表为几种物质的溶度积。
某同学设计了如下除杂方案:
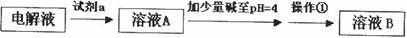
试剂a是__________ ,其目的是____________________________________ ;根据溶度积该方案能够除去的杂质金属阳离子是______ 。操作①用到的玻璃仪器是____________ 。
(4)工业上通常用FeS除去废水中的Cu2+,写出该沉淀转化离子方程式_____________
 6Cu+SO2↑,反应的氧化剂是
6Cu+SO2↑,反应的氧化剂是(2) 黄铜矿熔炼后得到的粗铜含少量Fe、Zn、Ag、Au等金属杂质,需进一步采用电解法精制。在电解精炼铜时,电解液中除了硫酸铜外,往往再加入一些硫酸,其作用是
(3)在精炼铜的过程中,电解液中c(Cu2+)逐渐下降,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。下表为几种物质的溶度积。
| 物质 | ||||
| 溶度积 |
某同学设计了如下除杂方案:
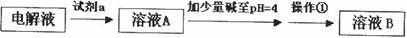
试剂a是
(4)工业上通常用FeS除去废水中的Cu2+,写出该沉淀转化离子方程式
I、通过火法治金炼出的铜是粗铜,含杂质金、银、铁、锌等金属和少量矿物杂质(与酸不反应)。制作电器及其他仪器产品时必须要求是纯铜,为此以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯。
表:几种物质形成沉淀时的pH
(1)在精炼铜时,阴极电极反应方程式为 ;金、银以单质的形式沉积在电解槽 (填“阳极”或“阴极”)的槽底。
(2)在精炼铜的过程中,Cu2+浓度逐渐降低,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。甲同学设计了如下除杂流程:

①试剂a最好选用 (填写序号),加入试剂a的目的是 。a、氯水 b、高锰酸钾溶液 c、硝酸 d、双氧水
②操作①是 ,根据上表数据分析,除杂方案中能够除去的杂质金属阳离子是
(填化学式)。
II、重金属离子对河流海洋等会造成严重的污染。某化工厂产生的废水(pH=2.0,密度为1g·mL-1)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01mol·L-1,排放前拟用沉淀法回收这两种金属,查找有关数据如下:
(1)你认为往废水中投入 (填字母序号)沉淀的效果最好
a、NaOH b、Na2S c、KI d、Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
表:几种物质形成沉淀时的pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀时的pH | 7.6 | 2.7 | 5.7 | 4.7 |
| 完全沉淀时的pH | 9.7 | 3.7 | 8.5 | 7.3 |
(2)在精炼铜的过程中,Cu2+浓度逐渐降低,c(Fe2+)、c(Zn2+)会逐渐增大,所以需定时除去其中的Fe2+、Zn2+。甲同学设计了如下除杂流程:

|
②操作①是 ,根据上表数据分析,除杂方案中能够除去的杂质金属阳离子是
(填化学式)。
II、重金属离子对河流海洋等会造成严重的污染。某化工厂产生的废水(pH=2.0,密度为1g·mL-1)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01mol·L-1,排放前拟用沉淀法回收这两种金属,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
a、NaOH b、Na2S c、KI d、Ca(OH)2
(2)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


