解答题-原理综合题 适中0.65 引用1 组卷129
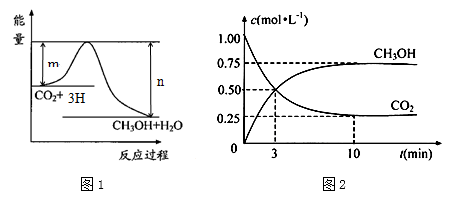
实现“节能减排”和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源.目前工业上有一种方法是用CO2来生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),图1表示该反应过程中能量变化:
CH3OH(g)+H2O(g),图1表示该反应过程中能量变化:

(1)关于该反应的下列说法中,正确的是__________(填字母).
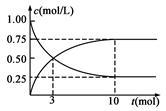
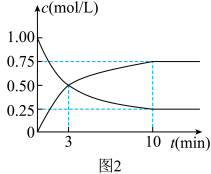
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),测得CO2和CH3O(g)的浓度随时间变化如图2所示.
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ mol/(L·min)
②该反应的平衡常数表达式K=______________
③下列措施中能使化学平衡向正反应方向移动的是__________ (填字母)
A.升高温度 B.将CH3OH(g)及时液化抽出 C.选择高效催化剂
(3)25℃,1.01105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:______________________ 。

(1)关于该反应的下列说法中,正确的是__________(填字母).
| A.△H>0,△S>0 | B.△H>0,△S<0 |
| C.△H<0,△S<0 | D.△H<0,△S>0 |
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②该反应的平衡常数表达式K=
③下列措施中能使化学平衡向正反应方向移动的是
A.升高温度 B.将CH3OH(g)及时液化抽出 C.选择高效催化剂
(3)25℃,1.01105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:
15-16高三上·江西上饶·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
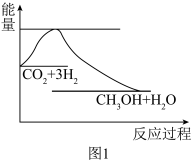
 CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。
CH3OH(g)+H2O(g),图1表示该反应进行过程中能量(单位为kJ·mol—1)的变化。