解答题-工业流程题 较难0.4 引用1 组卷219
中国有广阔的海岸线,海水的综合利用大有可为,海水中溴含量约为65mg/L,从海水中提取Br2的工艺流程如下:
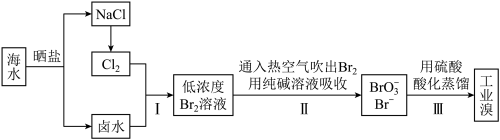
(1)①从海水中获得淡水的方法主要有_________ (填一种)
②我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为_________ 价。
(2)经过化学变化才能从海水中获得的物质是__________(选填字母序号)
(3)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的___________;
(4)请写出步骤Ⅱ中反应的离子反应方程式__________ 。

(1)①从海水中获得淡水的方法主要有
②我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为
(2)经过化学变化才能从海水中获得的物质是__________(选填字母序号)
| A.氯、溴、碘 | B.钠、镁 | C.烧碱、氢气 | D.食盐、淡水 |
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
15-16高一上·福建泉州·期末
类题推荐
茫茫大海是化学元素溴的“故乡”,海水中溴的含量约为67 mg/L。从海水中提取溴的工业流程如下:
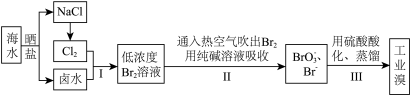
(1)步骤I中已获得了游离态的溴,步骤II中又将之转变成化合态的溴,其目的是_______ 。
(2)步骤II中通入热空气或水蒸气吹出Br2,利用了溴的______(填字母)。
(3)上述流程中吹出的溴蒸气也可先用SO2水溶液吸收,反应生成HBr和H2SO4,该反应中的氧化剂是________ , 还原剂是_______ ,然后用氯气氧化上述反应的产物后蒸馏,写出氯气氧化HBr的离子方程式:____________ 。

(1)步骤I中已获得了游离态的溴,步骤II中又将之转变成化合态的溴,其目的是
(2)步骤II中通入热空气或水蒸气吹出Br2,利用了溴的______(填字母)。
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(3)上述流程中吹出的溴蒸气也可先用SO2水溶液吸收,反应生成HBr和H2SO4,该反应中的氧化剂是
从海水中可以获得淡水、食盐并可提取镁和溴等物质。
(1)海水淡化的方法主要有___________ (填一种)。
(2)经过化学变化才能从海水中获得的物质是____________(填序号)
(3)从海水中提取镁的流程如下图所示:
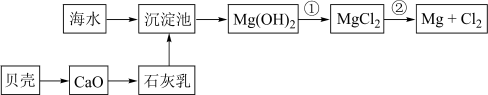
反应①的离子方程式为_______________________ 。
反应②的化学方程式为_______________________ 。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式为_____________________ 。
(1)海水淡化的方法主要有
(2)经过化学变化才能从海水中获得的物质是____________(填序号)
| A.氯、溴、碘 | B.钠、镁、铝 |
| C.烧碱、氢气 | D.食盐、淡水 |

反应①的离子方程式为
反应②的化学方程式为
(4)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



