解答题-实验探究题 适中0.65 引用1 组卷237
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等。
I.制备
称取14.0gCuSO4·5H2O、16.0gNa2CO3∙10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“滋滋”声,而且混合物很快成为“黏胶状”。将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含 为止,取出沉淀,风干,得到蓝绿色晶体。
为止,取出沉淀,风干,得到蓝绿色晶体。
(1)①混合物发生反应时有“滋滋”声的原因是____________ 。
②检验生成物已洗涤干净的方法是___________________________ 。
Ⅱ.组成测定
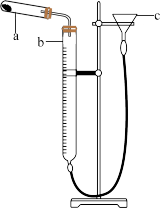
有同学查阅资料发现用Cu(OH)2∙CuCO3表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2∙nCuCO3,不同来源的碱式碳酸铜的m、n值需要具体测定。热分解法测定碱式碳酸铜组成的实验装置如图所示。通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值。
(2)①仪器b的名称是____________ 。②检查装置气密性的方法是______________ 。
③三次平行实验测定结果如下表,则该样品中m:n=_____________ ,若量气管中所盛液体为水,则该测定值比理论值___ (填“偏大”、“偏小”或“不变”)。
I.制备
称取14.0gCuSO4·5H2O、16.0gNa2CO3∙10H2O,用研钵分别研细后再混合研磨,立即发生反应,有“滋滋”声,而且混合物很快成为“黏胶状”。将混合物迅速投入200mL沸水中,快速搅拌并撤离热源,有蓝绿色沉淀生成,过滤,用水洗涤,至滤液中不含

(1)①混合物发生反应时有“滋滋”声的原因是
②检验生成物已洗涤干净的方法是
Ⅱ.组成测定
有同学查阅资料发现用Cu(OH)2∙CuCO3表示碱式碳酸铜是不准确的,较为准确、科学的表达式是mCu(OH)2∙nCuCO3,不同来源的碱式碳酸铜的m、n值需要具体测定。热分解法测定碱式碳酸铜组成的实验装置如图所示。通过测定碱式碳酸铜在灼热后所产生的气体体积,推导出碱式碳酸铜中碳酸铜和氢氧化铜的含量,即可求出m和n的比值。
(2)①仪器b的名称是
③三次平行实验测定结果如下表,则该样品中m:n=
实验序号 | 样品质量/g | CO2体积/mL(以折算成标准状况下) |
1 | 0.542 | 44.82 |
2 | 0.542 | 44.80 |
3 | 0.542 | 44.78 |
15-16高三下·湖南长沙·阶段练习
类题推荐
碱式碳酸铜[Cu(OH)2•CuCO3]是一种用途广泛的化工产品,实验室制备碱式碳酸铜的反应原理为:2CuSO4+2Na2CO3+H2O=Cu(OH)2•CuCO3↓+CO2↑+2Na2SO4。回答下列问题:
(1)配制100mL浓度均为0.50mol•L-1的CuSO4溶液和Na2CO3溶液,需要用到的玻璃仪器有量筒、烧杯、胶头滴管和___ 。
(2)取50mL0.50mol•L-1CuSO4溶液加入50mL0.50mol•L-1Na2CO3溶液中,反应后烧杯底部出现大量蓝绿色沉淀。设计实验证明蓝绿色沉淀中混有难溶于水的碱式硫酸铜[Cu2(OH)2SO4],实验步骤是:过滤,___ 。
(3)按最佳配比 n(CuSO4)︰n(Na2CO3)=1︰1.2进行实验,反应15min,所得实验结果如下:
分析75℃时沉淀量最多的原因:___ 。
(4)查阅资料可知碱式碳酸铜的组成有多种,可用xCu(OH)2•yCuCO3表示。某小组利用以下装置测定某碱式碳酸铜样品的组成:

①A中发生反应的化学方程式是___ 。
②加热时持续通入N2的目的是___ 。
③称取32.0g样品,充分反应后得到24.0g残留物,B增重3.6g,C增重4.4g。该样品的化学式为___ 。若对调B和C装置的位置,___ (填“能”或“不能”)测算出该样品的化学式。
(1)配制100mL浓度均为0.50mol•L-1的CuSO4溶液和Na2CO3溶液,需要用到的玻璃仪器有量筒、烧杯、胶头滴管和
(2)取50mL0.50mol•L-1CuSO4溶液加入50mL0.50mol•L-1Na2CO3溶液中,反应后烧杯底部出现大量蓝绿色沉淀。设计实验证明蓝绿色沉淀中混有难溶于水的碱式硫酸铜[Cu2(OH)2SO4],实验步骤是:过滤,
(3)按最佳配比 n(CuSO4)︰n(Na2CO3)=1︰1.2进行实验,反应15min,所得实验结果如下:
| 温度/℃ | 60 | 65 | 75 | 80 | 90 |
| 沉淀量/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
分析75℃时沉淀量最多的原因:
(4)查阅资料可知碱式碳酸铜的组成有多种,可用xCu(OH)2•yCuCO3表示。某小组利用以下装置测定某碱式碳酸铜样品的组成:

①A中发生反应的化学方程式是
②加热时持续通入N2的目的是
③称取32.0g样品,充分反应后得到24.0g残留物,B增重3.6g,C增重4.4g。该样品的化学式为
碱式碳酸铜可用作木材防腐剂、水体杀藻剂等,研究性学习小组设计以下方案制备碱式碳酸铜并进行相关实验探究。
Ι.以铜屑为原料制备碱式碳酸铜的装置如下:
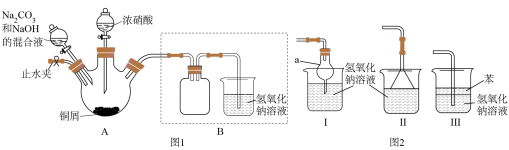
步骤1连接好装置,检查装置的气密性,装药品。
步骤2往三颈烧瓶中加入适量的浓硝酸,使铜屑完全反应。
步骤3往步骤2反应后的溶液中加入一定比例的Na2CO3和NaOH的混合液,加热。
步骤4将三颈烧瓶中的混合物过滤、洗涤、烘干,获得产物。
已知:ⅰ.碱式碳酸铜为草绿色或绿色结晶物,易溶于酸,不溶于水,在100℃的水中易分解;
ⅱ.NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO3+NaNO2+H2O;
NO不能单独与NaOH溶液反应。
(1)步骤2中浓硝酸与铜屑反应的离子方程式为___________________ 。
(2)步骤2反应一段时间后,须打开止水夹,通入一段时间的空气,目的是_______ 。
(3)步骤3对装置A的加热方式最好采用____________ 。
(4)装置Ι中仪器a的名称为____ ,Ⅰ、Ⅱ、Ⅲ三个装置不能替代图1中B装置的是_____ (填装置序号)。
(5)欲检验步骤4获得的产物中是否含有NO3-,所需的试剂可以是__________ 。
Ⅱ.探究在一定温度下,不同的原料配比对产物的影响,实验数据如下:
注:“+”越多表示沉淀量越多
(6)分析表格数据可得:制备碱式碳酸铜最佳的原料配比n[Cu(NO3)2]:n(NaOH) : n(Na2CO3) =___ 。
Ⅲ.产物组成的测定
(7)碱式碳酸铜的成分有多种,化学式可表示为mCu(OH)2·n CuCO3。为测定Ι中所得碱式碳酸铜的组成,学习小组同学准确称取3.820 g样品溶于适量的硫酸中,加水配成l00 mL溶液,取l0.00 mL溶液于锥形瓶中,加适量水稀释,调节溶液pH至3~4,加入过量的KI(2 Cu2++ 4 I-= 2 CuI↓ + I2),用0.l000 mol·L-1Na2S2O3标准溶液滴定(2 S2O32-+ I2= 2I-+ S4O62-),接近终点时,加入淀粉指示剂,继续滴定至终点,蓝色消失。进行平行实验后,测得平均消耗Na2S2O3标准溶液的体积为35.00 mL。该碱式碳酸铜的化学式为_____
Ι.以铜屑为原料制备碱式碳酸铜的装置如下:

步骤1连接好装置,检查装置的气密性,装药品。
步骤2往三颈烧瓶中加入适量的浓硝酸,使铜屑完全反应。
步骤3往步骤2反应后的溶液中加入一定比例的Na2CO3和NaOH的混合液,加热。
步骤4将三颈烧瓶中的混合物过滤、洗涤、烘干,获得产物。
已知:ⅰ.碱式碳酸铜为草绿色或绿色结晶物,易溶于酸,不溶于水,在100℃的水中易分解;
ⅱ.NO+NO2+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO3+NaNO2+H2O;
NO不能单独与NaOH溶液反应。
(1)步骤2中浓硝酸与铜屑反应的离子方程式为
(2)步骤2反应一段时间后,须打开止水夹,通入一段时间的空气,目的是
(3)步骤3对装置A的加热方式最好采用
(4)装置Ι中仪器a的名称为
(5)欲检验步骤4获得的产物中是否含有NO3-,所需的试剂可以是
Ⅱ.探究在一定温度下,不同的原料配比对产物的影响,实验数据如下:
| 实验序号 | V[Cu(NO3)2] /mL (0.5 mol·L-1) | V(NaOH) / mL (0.5 mol·L-1) | V(Na2CO3)/ mL (0.25 mol·L-1) | 沉淀数量 | 沉淀颜色 |
| 1 | 2.0 | 2.0 | 1.6 | + | 浅绿色 |
| 2 | 2.0 | 2.0 | 2.0 | + + | 浅绿色 |
| 3 | 2.0 | 2.0 | 2.4 | + + + | 蓝色 |
| 4 | 2.0 | 2.0 | 2.8 | + + + | 蓝色 |
(6)分析表格数据可得:制备碱式碳酸铜最佳的原料配比n[Cu(NO3)2]:n(NaOH) : n(Na2CO3) =
Ⅲ.产物组成的测定
(7)碱式碳酸铜的成分有多种,化学式可表示为mCu(OH)2·n CuCO3。为测定Ι中所得碱式碳酸铜的组成,学习小组同学准确称取3.820 g样品溶于适量的硫酸中,加水配成l00 mL溶液,取l0.00 mL溶液于锥形瓶中,加适量水稀释,调节溶液pH至3~4,加入过量的KI(2 Cu2++ 4 I-= 2 CuI↓ + I2),用0.l000 mol·L-1Na2S2O3标准溶液滴定(2 S2O32-+ I2= 2I-+ S4O62-),接近终点时,加入淀粉指示剂,继续滴定至终点,蓝色消失。进行平行实验后,测得平均消耗Na2S2O3标准溶液的体积为35.00 mL。该碱式碳酸铜的化学式为
碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2·yCuCO3。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3,某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol·L-1的Cu(NO3)2溶液、2.0mL 0.50 mol·L-1的NaOH溶液和0.25 mol·L-1的Na2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
①实验室制取少许孔雀石,应该采用的条件是___________ 。
②80℃时,所制得的孔雀石有少量褐色物质的原因是___________ 。
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
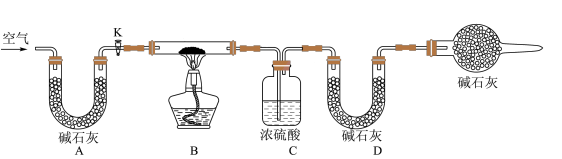
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:___________ 。
步骤5:称量相关装置的质量。
①装置A的作用是___________ ;若无装置E,则实验测定的x/y的值将___________ (选填“偏大”、“偏小”或“无影响”)。
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的___________ (写出所有组合的字母代号)一组即可进行计算,并根据你的计算结果,写出该样品组成的化学式___________ 。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3,某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol·L-1的Cu(NO3)2溶液、2.0mL 0.50 mol·L-1的NaOH溶液和0.25 mol·L-1的Na2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
| 编号 | V (Na2CO3)/ mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) | |
表Ⅰ | 表Ⅱ | |||||
②80℃时,所制得的孔雀石有少量褐色物质的原因是
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:

步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:
步骤5:称量相关装置的质量。
①装置A的作用是
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


