填空题 较难0.4 引用1 组卷55
在20 L的恒容密闭容器中,加入3 mol SO3(g)和1 mol氧气,在某温度下使其反应,反应至4 min时,氧气的浓度为0.06 mol/L,反应至8 min时达平衡状态。
(1)在0~4 min内生成O2的平均速率v(O2)=___ mol/(L·min)。
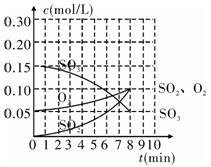
(2)整个过程中,各物质的浓度与时间的关系如图所示,则该温度下的平衡常数K=______ 。
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.05 mol/L的是______ ,此时的平衡常数与(2)中相比________ (填“增大”、“减小”或“不变”)。

(1)在0~4 min内生成O2的平均速率v(O2)=
(2)整个过程中,各物质的浓度与时间的关系如图所示,则该温度下的平衡常数K=
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.05 mol/L的是
| 选项 | A | B | C | D |
| SO3 | 1 mol | 3 mol | 3 mol | 0 mol |
| SO2 | 2 mol | 1.5 mol | 0 mol | 6 mol |
| O2 | 2 mol | 1 mol | 0 mol | 5 mol |
15-16高二上·湖南衡阳·期中
类题推荐
恒温下,在容积为2L的恒容密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g)ΔH<0,n(SO2)随时间变化关系如表:
2SO3(g)ΔH<0,n(SO2)随时间变化关系如表:
下列说法正确的是( )
 2SO3(g)ΔH<0,n(SO2)随时间变化关系如表:
2SO3(g)ΔH<0,n(SO2)随时间变化关系如表:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.2 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A.当容器中气体的密度不变时,该反应达到平衡状态 |
| B.用SO3表示0~4min内该反应的平均速率为0.01mol/(L·min) |
| C.升高温度时,逆反应速率大于正反应速率,平衡常数K值会减小 |
| D.平衡时再通入18O2,平衡右移,达新平衡时,18O仅存在于O2和SO3中 |
SO2催化氧化制SO3是工业制硫酸的关键过程,其反应为2SO2(g)+O2(g) 2SO3(g) △H<0。实验室模拟合成SO3,向温度为400℃,容积为0.5L的恒容密闭容器中加入2molSO2和1molO2,反应过程中SO3浓度随时间变化情况见表。
2SO3(g) △H<0。实验室模拟合成SO3,向温度为400℃,容积为0.5L的恒容密闭容器中加入2molSO2和1molO2,反应过程中SO3浓度随时间变化情况见表。
(1)0~3min内SO2的平均反应速率为____ mol·L-1·min-1,5min后若改变某一条件使得SO3的浓度发生了如表所示的变化,则该条件为___ (填标号)。
A.升高温度 B.增大SO2浓度 C.移出部分SO3 D.降低温度 E.加入合适的催化剂
(2)判断该反应达到平衡状态的依据是____ (填标号)。
A.2v正(SO3)=v逆(O2)
B.气体的平均相对分子质量不再改变
C.气体的密度不再改变
(3)4min时保持其他条件不变,若再向容器中通入0.5molSO2和0.5molSO3,则平衡将向____ (填“正”或“逆”)反应方向移动。
(4)4min时保持其他条件不变,仅充入氮气,使体系压强增大,SO2转化率将___ (填“变大”、“变小”或“不变”)。
(5)若初始投料及其他条件不变,在温度为T2℃时进行反应,达到新平衡后,气体总压强是反应前的 ,则SO2的物质的量分数为
,则SO2的物质的量分数为____ ,T2℃时的平衡常数K为___ ,T2____ (填“=”或“<”)400℃。
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| SO3浓度/(mol·L-1) | 1.2 | 2.0 | 2.7 | 3.0 | 3.0 | 2.4 | 2.1 | 2.1 |
(1)0~3min内SO2的平均反应速率为
A.升高温度 B.增大SO2浓度 C.移出部分SO3 D.降低温度 E.加入合适的催化剂
(2)判断该反应达到平衡状态的依据是
A.2v正(SO3)=v逆(O2)
B.气体的平均相对分子质量不再改变
C.气体的密度不再改变
(3)4min时保持其他条件不变,若再向容器中通入0.5molSO2和0.5molSO3,则平衡将向
(4)4min时保持其他条件不变,仅充入氮气,使体系压强增大,SO2转化率将
(5)若初始投料及其他条件不变,在温度为T2℃时进行反应,达到新平衡后,气体总压强是反应前的
在一定温度下,将4.0 mol SO2与2.0 mol O2的混合气体充入容积为2 L的密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g),经过2 min达到平衡状态,SO2的平衡转化率90.0%。
2SO3(g),经过2 min达到平衡状态,SO2的平衡转化率90.0%。
(1)下列关于反应2SO2(g)+O2(g) 2SO3(g)的描述正确的是
2SO3(g)的描述正确的是
(2)0~2 min内O2的平均反应速率v(O2)=___________
(3)该温度下此反应的化学平衡常数的值K=___________
(4)在相同温度下,某容器内c(SO2) = c(O2) = c(SO3) = 1.0 mol·L-1, 则此时反应速率 v(正)___________ v(逆) (填“>”、“<”或“=”)
(5)在一定温度下,下列措施可以提高SO2转化率的是___________(填字母)。
(1)下列关于反应2SO2(g)+O2(g)
| A.增大O2的浓度,该反应的平衡常数增大 |
| B.若2v正(SO2)=v逆(O2) ,则反应达到平衡状态 |
| C.压缩体积,正反应速率增大,逆反应速率减小 |
| D.在其他条件不变时,升高温度能提高活化分子百分数,反应速率增大 |
(3)该温度下此反应的化学平衡常数的值K=
(4)在相同温度下,某容器内c(SO2) = c(O2) = c(SO3) = 1.0 mol·L-1, 则此时反应速率 v(正)
(5)在一定温度下,下列措施可以提高SO2转化率的是___________(填字母)。
| A.增大SO2的浓度 | B.容积不变,充入氖气 |
| C.增大O2的浓度 | D.容积不变,再充入4.0 mol SO2与2.0 mol O2 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


