解答题-实验探究题 适中0.65 引用1 组卷165
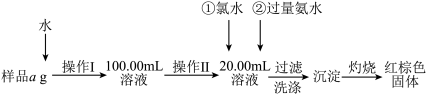
氯化铁是常见的水处理剂。某氯化铁(FeCl3·6H2O)样品含有少量FeCl2杂质。现要测定其中FeCl3·6H2O的质量分数,实验按以下步骤进行:
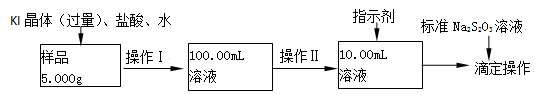
已知有关离子方程式为:2Fe3+ +2I-==2Fe2++ I2 , I2+2S2O32-==2I- +S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻液体呈现红褐色,反应的离子方程式为:__________________ 。
(2)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有____________ 、___________ (填仪器名称)。
(3)操作Ⅱ必须用到的仪器是_______________ (选填编号);
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
(4)指示剂是淀粉溶液,则达到滴定终点的现象是___________________ 。
(5)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3 溶液18.17mL。该样品中FeCl3·6H2O的质量分数为____________________ 。
(6)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是______________ (选填编号)。
a.铁粉 b.氯水 c.溴水 d.双氧水

已知有关离子方程式为:2Fe3+ +2I-==2Fe2++ I2 , I2+2S2O32-==2I- +S4O62-
(1)取少量氯化铁样品滴入50mL沸水中,加热片刻液体呈现红褐色,反应的离子方程式为:
(2)操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有
(3)操作Ⅱ必须用到的仪器是
a.50mL烧杯 b.10mL量筒 c.20mL量筒 d.25mL滴定管
(4)指示剂是淀粉溶液,则达到滴定终点的现象是
(5)滴定时,消耗浓度为0.1000mol/L的标准Na2S2O3 溶液18.17mL。该样品中FeCl3·6H2O的质量分数为
(6)要把样品氯化铁中的少量FeCl2杂质除去,可用的试剂是
a.铁粉 b.氯水 c.溴水 d.双氧水
15-16高二上·河南三门峡·期中
类题推荐
某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
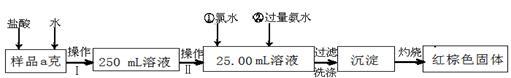
请根据上面流程,回答以下问题:
(1)操作I 所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有_______ (填自选仪器名称),操作II 必须用到的仪器是_______ (从以下选项中选择,填编号)。
(2)加入试剂①和②后发生反应的离子反应方程式为:_______
(3)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3 g,则接下来还应进行的操作是_______ 。
(4) 若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:_______ 。
(5) 有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是:
_______ (用化学方程式表示)

请根据上面流程,回答以下问题:
(1)操作I 所用到的玻璃仪器除烧杯、玻璃棒、量筒外,还必须有
| A.50mL烧杯 | B.50mL量筒 | C.25mL碱式滴定管 | D.25mL酸式滴定管 |
(2)加入试剂①和②后发生反应的离子反应方程式为:
(3)将沉淀物加热,并置于干燥器中冷却至室温,用天平称量其质量为b1g,再次加热并冷却至室温称量其质量为b2 g,若b1-b2=0.3 g,则接下来还应进行的操作是
(4) 若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数是:
(5) 有同学认为:上述流程中若不加入氯水,其它步骤不变,仍可达到目的。他的理由是:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网