填空题 较难0.4 引用1 组卷198
铜是过渡元素。化合物中,铜常呈现+1价或+2价。
(1)铜原子的原子结构示意图:_________________ ;
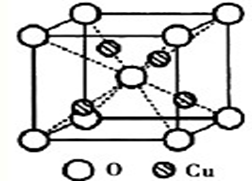
(2)右图为某铜矿晶体结构单元,该铜矿的化学式为____________________ 。
(3)已知,铜的第一电离能为746kJ·mol-1,第二电离能为1958kJ·mol-1。请结合核外电子排布相关知识解释,铜第二电离能远远大于第一电离能的原因:___________________ 。
(4)对于CuX(X为卤素)而言,铜与X形成的化学键极性越强,对应的CuX的溶解度越大。据此可知,CuCl的溶解度比CuI的溶解度__________ (填“更大”或“更小”);
(5)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为[Cu(NH3)n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对。
①[Cu(NH3)n]+中n =______________________ ;
②[Cu(NH3)n]+中Cu+与n个氮原子构成的空间结构呈________________ 型;
③[Cu(NH3)n]+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO。加热分解放出CO的过程中,必须克服微粒间的作用力是______________ 。
(6)+2价铜的氢氧化物难溶于水,但可溶于浓氨水形成配位数为4的配合物。写出氢氧化铜溶解于浓氨水的离子方程式_____________________ 。

(1)铜原子的原子结构示意图:
(2)右图为某铜矿晶体结构单元,该铜矿的化学式为
(3)已知,铜的第一电离能为746kJ·mol-1,第二电离能为1958kJ·mol-1。请结合核外电子排布相关知识解释,铜第二电离能远远大于第一电离能的原因:
(4)对于CuX(X为卤素)而言,铜与X形成的化学键极性越强,对应的CuX的溶解度越大。据此可知,CuCl的溶解度比CuI的溶解度
(5)CO、NH3都能提供孤电子对与Cu+形成配合物。Cu+与NH3形成的配合物可表示为[Cu(NH3)n]+。该配合物中,Cu+的4s轨道及4p轨道通过sp杂化接受NH3提供的孤电子对。
①[Cu(NH3)n]+中n =
②[Cu(NH3)n]+中Cu+与n个氮原子构成的空间结构呈
③[Cu(NH3)n]+溶液可用于吸收合成氨原料气中的CO,加热吸收CO后的溶液又将放出CO。加热分解放出CO的过程中,必须克服微粒间的作用力是
(6)+2价铜的氢氧化物难溶于水,但可溶于浓氨水形成配位数为4的配合物。写出氢氧化铜溶解于浓氨水的离子方程式
15-16高二上·山东淄博·期中
类题推荐
回答下列问题:
(1)铁单质及其化合物的应用非常广泛。
①基态Fe原子价电子排布图是_______ 。
②普鲁士蓝的化学式为Fe4[Fe(CN)6]3,碳原子与Fe2+形成配位键,其中提供孤电子对的是_______ (填元素符号),CN-与N2互为等电子体,1mol普鲁士蓝中所含 键的数目为
键的数目为 _______ 个。
③邻羟基苯甲醛 和对羟基苯甲醛
和对羟基苯甲醛  均能与
均能与 溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为
溶液反应生成紫色配合物。对羟基苯甲醛在水中的溶解度略大于邻羟基苯甲醛在水中的溶解度,原因为_______ 。
(2)硼酸(H3BO3)晶体具有与石墨相似的层状结构,如图所示:

①硼酸分子中B原子杂化轨道的类型为_______ ,1molH3BO3的晶体中有_______ mol氢键。
②以硼酸为原料可制得硼氢化钠(NaBH4),NaBH4的电子式为_______ 。
(3)CuCl的盐酸溶液吸收CO可生成配合物,其结构如图所示:

①氯原子的杂化方式为_______ 。
②该配合物中,每个Cu原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键_______ 。
③Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s及4p轨道通过sp杂化接受NH3提供的电子对,n=_______ 。
④已知NF3与NH3的空间构型相同,但NF3不易与Cu+形成配离子,其原因是_______ 。
⑤下表是铜与锌的部分离能数据,对于“铜的 I1与l2相差较大,而锌的I1与I2相差较小”的事实,原因是_______ 。
(4)Li2O是一种白色粉末,常用于特种玻璃、陶瓷、医药等领域。请回答下列问题:
①Li2O具有反萤石结构,其立方晶胞结构如图所示,A表示_______ (填“Li”或“O”),配位数是_______ 。

②若晶胞中M的坐标为(0,0,0),N的坐标为(1,1,1),则P的坐标为_______ 。
(1)铁单质及其化合物的应用非常广泛。
①基态Fe原子价电子排布图是
②普鲁士蓝的化学式为Fe4[Fe(CN)6]3,碳原子与Fe2+形成配位键,其中提供孤电子对的是
③邻羟基苯甲醛
 和对羟基苯甲醛
和对羟基苯甲醛  均能与
均能与(2)硼酸(H3BO3)晶体具有与石墨相似的层状结构,如图所示:

①硼酸分子中B原子杂化轨道的类型为
②以硼酸为原料可制得硼氢化钠(NaBH4),NaBH4的电子式为
(3)CuCl的盐酸溶液吸收CO可生成配合物,其结构如图所示:

①氯原子的杂化方式为
②该配合物中,每个Cu原子能与其他原子形成3个配位键,在图中用“→”标出相应的配位键
③Cu+与NH3形成的配合物可表示成[Cu(NH3)n]+,该配合物中,Cu+的4s及4p轨道通过sp杂化接受NH3提供的电子对,n=
④已知NF3与NH3的空间构型相同,但NF3不易与Cu+形成配离子,其原因是
⑤下表是铜与锌的部分离能数据,对于“铜的 I1与l2相差较大,而锌的I1与I2相差较小”的事实,原因是
| 电离能/kJ·mol-1 | I1 | I2 |
| Cu | 746 | 1958 |
| Zn | 906 | 1733 |
①Li2O具有反萤石结构,其立方晶胞结构如图所示,A表示

②若晶胞中M的坐标为(0,0,0),N的坐标为(1,1,1),则P的坐标为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 和对羟基苯甲醛
和对羟基苯甲醛  均能与
均能与



