填空题 适中0.65 引用8 组卷552
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该反应的离子方程式___________________________ 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是_____________ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_________________ <_____________ (填实验序号)。
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末, c( )=
)=__________ mol/L(假设混合液体积为50mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_____________ 来比较化学反应速率。(一条即可)
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

①__________________________ ;②__________________________ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1 H2C2O4溶液 | 30mL 0.01mol·L-1 KMnO4溶液 |
| ② | 20mL 0.2mol·L-1 H2C2O4溶液 | 30mL 0.01mol·L-1 KMnO4溶液 |
(1)该反应的离子方程式
(2)该实验探究的是
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末, c(
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

①
15-16高二上·江西南昌·阶段练习
类题推荐
Ⅰ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该实验探究的是_____________ 因素对化学反应速率的影响。如图一,相同时间内针筒中所得的CO2体积大小关系是____________ (填实验序号)。
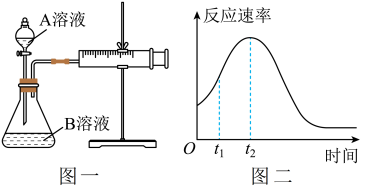
(2)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_____________________________________________ 来比较化学反应速率。
(3)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______________________________ 。
Ⅱ.(1)一定温度下,在容积2 L的密闭容器中充入3 mol A 气体和2.5 mol B气体,发生反应3A(g)+B(g) xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:
xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:
①A的平均消耗速率为_______ ;
②平衡时B的转化率为____________ ;
③X值为____________ ;
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
(1)该实验探究的是

(2)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(3)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
Ⅱ.(1)一定温度下,在容积2 L的密闭容器中充入3 mol A 气体和2.5 mol B气体,发生反应3A(g)+B(g)
 xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:
xC(g)+2D(g),经过5 min反应达平衡,生成1.0 mol D,同时测得C的平均生成速率为0.10 mol/(L·min),则:①A的平均消耗速率为
②平衡时B的转化率为
③X值为
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,一实验小组欲通过图1装置探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

(1)该反应中MnO4-被还原为Mn2+,写出相应反应的离子方程式:___ 。
(2)该实验探究的是___ 因素对化学反应速率的影响。针筒内收集相同体积的CO2,所用时间是①__ ②(填“>”、“<”或“=”)。
(3)本实验还可通过测定___ 来比较化学反应速率。
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变化的主要原因可能是___ 。
(5)图3中阴影部分“面积”还可以表示t1~t3时间内___ 。(填字母)
A.c(Mn2+)的增加量 B.n(Mn2+)的增加量
C.c(SO42-)的增加量 D.c(MnO4-)的增加量
| 实验序号 | A溶液 | B溶液 |
① | 20mL 0.1mol/L H2C2O4溶液 | 30mL 0.1mol/L KMnO4溶液 |
② | 20mL 0.2mol/L H2C2O4溶液 | 30mL 0.1mol/L KMnO4溶液 |

(1)该反应中MnO4-被还原为Mn2+,写出相应反应的离子方程式:
(2)该实验探究的是
(3)本实验还可通过测定
(4)小组同学发现反应速率总是如图2,其中t1~t2时间内速率变化的主要原因可能是
(5)图3中阴影部分“面积”还可以表示t1~t3时间内
A.c(Mn2+)的增加量 B.n(Mn2+)的增加量
C.c(SO42-)的增加量 D.c(MnO4-)的增加量
实验题
I.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2 + 5H2C2O4+6H+ =2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+ 5H2C2O4+6H+ =2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该实验探究的是_______ 因素对化学反应速率的影响。如图,相同时间内针筒中所得CO2的体积大小关系是_______ >_______ (填实验序号)。

(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c( )=
)=_______ mol·L-1(假设混合后溶液体积不变)
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(4)小组同学发现反应速率变化如图,其中t1~t2时间内速率变快的主要原因可能是
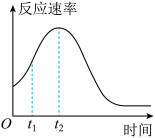
①该反应放热
②_______ 。
II.某小组同学欲探究 NH3的催化氧化实验,按如图装置进行实验。
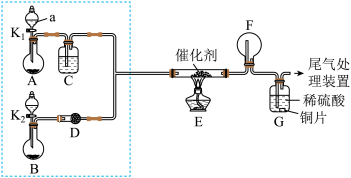
A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)制取NH3是在哪一装置中_______ (填 A 或 B)
(2)装置D中盛放的试剂可以是_______ (填序号)。
A.浓硫酸 B.碱石灰 C.无水氯化钙 D..硫酸铜
(3)装置E中发生反应的化学方程式为_______ 。
I.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2
| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL 0.1 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |
| ② | 20 mL 0.2 mol·L-1 H2C2O4溶液 | 30 mL 0.01 mol·L-1 KMnO4溶液 |

(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(4)小组同学发现反应速率变化如图,其中t1~t2时间内速率变快的主要原因可能是

①该反应放热
②
II.某小组同学欲探究 NH3的催化氧化实验,按如图装置进行实验。

A、B装置可选药品:浓氨水、H2O2、蒸馏水、NaOH固体、MnO2
(1)制取NH3是在哪一装置中
(2)装置D中盛放的试剂可以是
A.浓硫酸 B.碱石灰 C.无水氯化钙 D..硫酸铜
(3)装置E中发生反应的化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


