单选题 适中0.65 引用4 组卷263
向含2mol NaOH、1mol Ba(OH)2、2mol NaAlO2的混合液中慢慢通入CO2至过量,下列有关说法正确的是

| A.整个过程中共发生四个离子反应。 |
| B.根据现象可判断酸性强弱为:H2CO3>HAlO2>HCO3- |
| C.通入3molCO2和通入5molCO2都只产生3mol沉淀 |
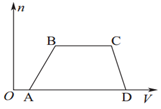
| D.整个过程中生成沉淀的物质的量与通入CO2的体积的图象如图所示: |
15-16高三上·江西南昌·阶段练习
类题推荐
向体积为2 L、物质的量浓度均为1mol/L的NH3·H2O、Ba(OH)2、KAlO2的混合溶液中缓缓地通入CO2至过量,则下列说法正确的是( )
A.整个过程中通入的CO2(x轴)与生成沉淀(y轴)的关系如图所示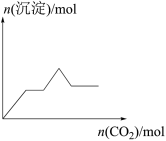 |
| B.当沉淀达到最大值时,至少通入标准状况下的CO2的体积为89.6L |
| C.缓缓通入CO2与KAlO2反应时的离子方程式为:AlO2-+CO2+2H2O===Al(OH)3↓+HCO3- |
| D.沉淀刚达到最大值时,溶液中离子浓度的关系为:c(K+)>c(CO32-)>c(OH-)>c(NH4+)>c(H+) |
将CO2气体缓缓地通入到含KOH、Ca(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是
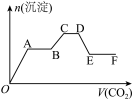
| A.D~E段沉淀减少的反应方程式是:CaCO3 + CO2 + H2O = Ca(HCO3)2 |
| B.A~B段与C~D段发生反应的离子方程式都是:CO32- + CO2+H2O =2HCO3- |
| C.B~C段反应的离子方程式是:Ca(OH)2+CO2=CaCO3↓+H2O |
| D.O~A段反应的化方程式是:2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32- |
标准状况下将 气体缓缓地通入到含2molKOH、
气体缓缓地通入到含2molKOH、 和
和 的混合溶液中直至过量,生成沉淀的物质的量与所通
的混合溶液中直至过量,生成沉淀的物质的量与所通 的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是
的体积关系如图所示。下列关于整个反应进程中的各种描述正确的是
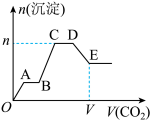

| A. |
| B. |
| C. |
| D.D点所得溶液中离子浓度的关系为: |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


