解答题-实验探究题 适中0.65 引用1 组卷375
NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为 ;该反应发生、气体收集和尾气处理装置依次为 。
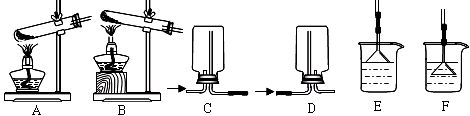
(2)按下图装置进行NH3性质实验。
先打开旋塞1,B瓶中的现象是 ,稳定后,关闭旋塞1。再打开旋塞2,B瓶中的现象是 。
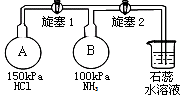
(3)写出NH4Cl溶液水解的离子方程式 。
设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限选试剂与仪器:固体NH4Cl、蒸馏水、250mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究 对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积)。
③按实验序号1所拟数据进行实验,若读取的待测物理量的数值为X,则NH4Cl水解反应的平衡转化率为 (只列出算式,忽略水自身电离的影响)。
(1)用NH4Cl和Ca(OH)2制备NH3的化学方程式为 ;该反应发生、气体收集和尾气处理装置依次为 。

(2)按下图装置进行NH3性质实验。
先打开旋塞1,B瓶中的现象是 ,稳定后,关闭旋塞1。再打开旋塞2,B瓶中的现象是 。

(3)写出NH4Cl溶液水解的离子方程式 。
设计实验,探究某一种因素对溶液中NH4Cl水解程度的影响。
限选试剂与仪器:固体NH4Cl、蒸馏水、250mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可调控温度)
①实验目的:探究 对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中“V(溶液)”表示所配制溶液的体积)。
| 物理量 实验序号 | V(溶液)/mL | NH4Cl质量/g | 温度/℃ | …… | |
| 1 | 250 | X | …… | ||
| 2 | 250 | …… |
2015·安徽·一模
类题推荐
1.氨气是一种重要的工业原料。
(1)氨气的制备

①氨气的发生装置可以选择上图中的_______ ,反应的化学方程式为_______ 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→_______ (按气流方向,用小写字母表示)。
③新制的氨水中含氮元素的微粒有3种: 、
、 和
和 ,试用合理的方程式解释:
,试用合理的方程式解释:_______ 。
(2)设计实验,探究 对稀氨水中存在的溶质的电离平衡的影响。
对稀氨水中存在的溶质的电离平衡的影响。
已知:影响电离平衡的因素有浓度、温度等。
①限制试剂与仪器:0.1mol/L氨水、 、
、 、
、 、
、 、量筒、烧杯、玻璃棒、药匙、天平、pH计、恒温水浴槽(可控制温度)。
、量筒、烧杯、玻璃棒、药匙、天平、pH计、恒温水浴槽(可控制温度)。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量,数据用字母表示)。
③表中物理量“m(铵盐)/g”的铵盐是_______ (填字母)。
A. B.
B. C.
C. D.
D.
(已知25℃几种弱电解质的电离常数分别为:
 、醋酸
、醋酸 、碳酸
、碳酸 和
和 )
)
④按实验序号2所拟数据进行实验,则一水合氨的电离度(平衡转化率)为_______ 。(可忽略水的电离)
(1)氨气的制备

①氨气的发生装置可以选择上图中的
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→
③新制的氨水中含氮元素的微粒有3种:
(2)设计实验,探究
已知:影响电离平衡的因素有浓度、温度等。
①限制试剂与仪器:0.1mol/L氨水、
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量,数据用字母表示)。
| 物理量 实验序号 | V(0.1mol/L氨水)/mL | m(铵盐)/g | …… | ||
| 1 | 100 | 0 | …… | ||
| 2 | 100 | a | …… |
A.
(已知25℃几种弱电解质的电离常数分别为:
④按实验序号2所拟数据进行实验,则一水合氨的电离度(平衡转化率)为
氨气是一种重要的工业原料。
(1)氨气的制备
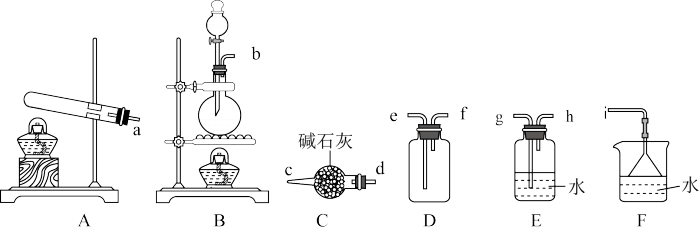
①氨气的发生装置可以选择上图中的_______ ,反应的化学方程式为_______ 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→_______ (按气流方向,用小写字母表示)。
③新制的氨水中含氮元素的微粒有3种: 、
、 和
和 ,试用合理的方程式解释:
,试用合理的方程式解释:_______ 。
(2)设计实验,探究 对稀氨水中存在的溶质的电离平衡的影响。
对稀氨水中存在的溶质的电离平衡的影响。
①限制试剂与仪器:0.1mol/L氨水、 、
、 、
、 、
、 、量筒、烧杯、玻璃棒、药匙、天平、pH计、恒温水浴槽(可控制温度)。
、量筒、烧杯、玻璃棒、药匙、天平、pH计、恒温水浴槽(可控制温度)。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量)。
③表中物理量“m(铵盐)/g”的铵盐是_______ 。(已知25℃几种弱电解质的电离常数分别为:
 、醋酸
、醋酸 、碳酸
、碳酸 和
和 )
)
④按实验序号2所拟数据进行实验,则一水合氮的电离度(平衡转化率)为_______ 。
(1)氨气的制备

①氨气的发生装置可以选择上图中的
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→
③新制的氨水中含氮元素的微粒有3种:
(2)设计实验,探究
①限制试剂与仪器:0.1mol/L氨水、
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量)。
物理量 实验序号 | V(0.1mol/L氨水)/mL | m(铵盐)/g | t/℃ | |
| 1 | 100 | 0 | 25 | b |
| 2 | 100 | a | 25 | c |
④按实验序号2所拟数据进行实验,则一水合氮的电离度(平衡转化率)为
NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为________ 、________ 、_______ (填字母)。

(2)恒定温度下在特制的密闭真空容器中充入2molNH3、1molCO2,发生反应制备氨基甲酸铵 2NH3(g)+CO2(g) NH2COONH4(s)(假设固体试样体积忽略不计)。若容器体积不变,可以判断该反应已经达到化学平衡的是
NH2COONH4(s)(假设固体试样体积忽略不计)。若容器体积不变,可以判断该反应已经达到化学平衡的是________ (填字母)。
A.υ(NH3)= 2υ(CO2) B.密闭容器中总压强不变 C. 密闭容器中混合气体的密度不变
上述反应达到平衡后,若在恒温下压缩容器体积,重新达平衡后混合气体中NH3的体积分数____________ (填“增加”、“减小”或“不变”)。
(3)铵盐在水溶液中建立如下水解平衡:NH4Cl+H2O NH3·H2O+HCl,研究表明,浓度、温度、pH均对铵盐水解程度(即上述反应中NH4Cl的转化率)产生影响。某兴趣小组探究某一种因素对溶液中NH4Cl水解程度的影响。
NH3·H2O+HCl,研究表明,浓度、温度、pH均对铵盐水解程度(即上述反应中NH4Cl的转化率)产生影响。某兴趣小组探究某一种因素对溶液中NH4Cl水解程度的影响。
试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)。
设计实验方案,pH为拟测定的数据,表中V(溶液)表示所配制NH4Cl溶液的体积。
请分析,实验1、2的目的是探究______________ 对溶液中NH4Cl水解程度的影响,实验2、3的目的是探究_____________ 对溶液中NH4Cl水解程度的影响。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为

(2)恒定温度下在特制的密闭真空容器中充入2molNH3、1molCO2,发生反应制备氨基甲酸铵 2NH3(g)+CO2(g)
A.υ(NH3)= 2υ(CO2) B.密闭容器中总压强不变 C. 密闭容器中混合气体的密度不变
上述反应达到平衡后,若在恒温下压缩容器体积,重新达平衡后混合气体中NH3的体积分数
(3)铵盐在水溶液中建立如下水解平衡:NH4Cl+H2O
试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、pH计、温度计、恒温水浴槽(可控制温度)。
设计实验方案,pH为拟测定的数据,表中V(溶液)表示所配制NH4Cl溶液的体积。
| 物理量 实验序号 | V(溶液)/mL | NH4Cl /g | 温度/℃ | pH | … |
| 1 | 100 | m | T1 | … | |
| 2 | 100 | m | T2 | … | |
| 3 | 100 | 2m | T2 | … |
请分析,实验1、2的目的是探究
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


