填空题 较难0.4 引用2 组卷552
节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若宁波全市的140余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放量将近100万吨。常利用煤气化过程中生成的CO和H2来制备甲醇:CO+2H2 CH3OH。请根据图示回答下列问题:
CH3OH。请根据图示回答下列问题:
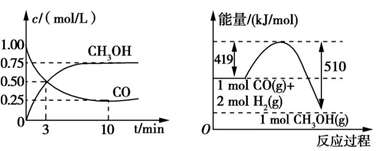
(1)关于该反应的下列说法中,正确的是____ (填字母)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0 D.ΔH<0,ΔS>0
(2)现进行如下实验:在体积为1 L的密闭容器中,充入1 mol CO和3 mol H2,测得CO和CH3OH(g)的浓度随时间变化如图1所示。从反应开始到反应达到平衡,CO的平均反应速率v(CO)=_____ ,该反应的平衡常数K=______ 。
(3)恒容条件下,达到平衡后,下列措施中能使n (CH3OH)/n(CO)增大的有______ 。
A.升高温度 B.充入气体He
C.再充入1 mol CO和3 mol H2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量为_____________ g/mol。
(5)根据图2,写出此反应的热化学方程式:________________ 。
 CH3OH。请根据图示回答下列问题:
CH3OH。请根据图示回答下列问题:
图1 图2
(1)关于该反应的下列说法中,正确的是
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0 D.ΔH<0,ΔS>0
(2)现进行如下实验:在体积为1 L的密闭容器中,充入1 mol CO和3 mol H2,测得CO和CH3OH(g)的浓度随时间变化如图1所示。从反应开始到反应达到平衡,CO的平均反应速率v(CO)=
(3)恒容条件下,达到平衡后,下列措施中能使n (CH3OH)/n(CO)增大的有
A.升高温度 B.充入气体He
C.再充入1 mol CO和3 mol H2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1 mol CO、2 mol H2和1 mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量为
(5)根据图2,写出此反应的热化学方程式:
15-16高三上·湖北黄石·阶段练习
类题推荐
节能减排已经成为全社会的共识,有一种思路是将一氧化碳(CO)转化成可燃物质甲醇,甲醇汽油能减少有害气体(CO)排放。现有一种利用煤气化过程中生成的CO和H2来制备甲醇的方案,其反应原理为:CO(g)+2H2(g) CH3OH(g)。请根据下列图示回答问题:
CH3OH(g)。请根据下列图示回答问题:
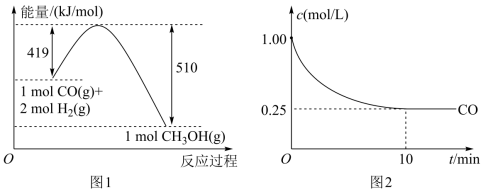
(1)根据(图1),写出此反应的热化学方程式___________ 。下列关于此反应的说法中,正确的是___________ (填字母)
A.任何条件都能自发进行 B.高温条件能够自发进行
C.任何条件都不自发进行 D.低温条件能够自发进行
(2)现进行如下实验,在体积为1L的密闭容器中,充入1
 和3
和3
 ,测得
,测得 的浓度随时间变化如(图2)所示,从反应开始到平衡,
的浓度随时间变化如(图2)所示,从反应开始到平衡, 的平均反应速率
的平均反应速率
___________ 
(3)恒容条件下,上述反应达到平衡后,以下措施中能使 增大的有___________。
增大的有___________。
(4)已知在常温常压下:化学反应①②的平衡常数分别为 ,
,
①2CH3OH(l)+O2(g) CO2(g)+4H2(g) K1
CO2(g)+4H2(g) K1
②2CO(g)+O2(g) CO2(g) K2
CO2(g) K2
则CO(g)+2H2(g) CH3OH(l)的
CH3OH(l)的
___________ (用含有K1,K2的代数式表达)

(1)根据(图1),写出此反应的热化学方程式
A.任何条件都能自发进行 B.高温条件能够自发进行
C.任何条件都不自发进行 D.低温条件能够自发进行
(2)现进行如下实验,在体积为1L的密闭容器中,充入1
(3)恒容条件下,上述反应达到平衡后,以下措施中能使
| A.升高温度 | B.充入 |
| C.再充入1 | D.使用催化剂 |
①2CH3OH(l)+O2(g)
②2CO(g)+O2(g)
则CO(g)+2H2(g)
甲醇可通过将煤的气化过程中生成的CO和H2在一定条件下发生如下反应制得:CO(g) + 2H2(g)=CH3OH(g)
请根据下图回答下列问题:
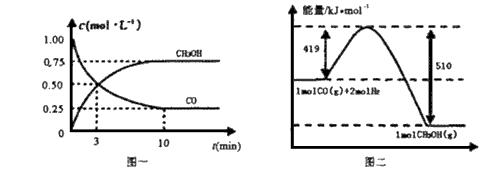
(1)从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=____mol / (L·min)。
(2)写出该反应的热化学方程式____________________________________________
(3)恒容条件下,下列措施中能使 n(CO) n(CH3OH)增大的有 。
A.升高温度 B.充入He气
C.再充入1 mol CO和2 mol H2 D.使用催化剂
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
则下列关系正确的是:
A. c1=c2
B.2Q1=Q3 ……
C.2a1=a3
D. a1+ a3=1
E.该反应若生成1 mol CH3OH,则放出(Q1+ Q2)kJ热量
(5)若在一体积可变的密闭容器中充入1molCO、2mol H2和1mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是由质量守恒,密度为原来的1.6倍,所以体积缩小,平衡正移。
请根据下图回答下列问题:

(1)从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=____mol / (L·min)。
(2)写出该反应的热化学方程式____________________________________________
(3)恒容条件下,下列措施中能使 n(CO) n(CH3OH)增大的有 。
A.升高温度 B.充入He气
C.再充入1 mol CO和2 mol H2 D.使用催化剂
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表:
| 容器 | 反应物投入的量 | 反应物的转化率 | CH3OH的浓度 | 能量变化(Q1、Q2、Q3均大于0) |
| 甲 | 1 mol CO和2 mol H2 | a1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | a2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4 mol H2 | a3 | c3 | 放出Q3kJ热量 |
则下列关系正确的是:
A. c1=c2
B.2Q1=Q3 ……
C.2a1=a3
D. a1+ a3=1
E.该反应若生成1 mol CH3OH,则放出(Q1+ Q2)kJ热量
(5)若在一体积可变的密闭容器中充入1molCO、2mol H2和1mol CH3OH,达到平衡时测得混合气体的密度是同温同压下起始的1.6倍,则该反应向 (填“正”、“逆”)反应方向移动,理由是由质量守恒,密度为原来的1.6倍,所以体积缩小,平衡正移。
甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇。
(1)已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为___ 。
(2)某研究性学习小组在容积固定为2L的密闭容器内充入1molCO和2molH2,加入合适催化剂(体积可以忽略不计)后进行反应CO(g)+2H2(g)=CH3OH(g) ΔH<0。
①下列措施中有利于增大该反应的反应速率且提高转化率的是__ (填字母序号)
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.使用高效催化剂 D.增大体系压强
②实验过程中用压力计监测容器内压强的变化如下:
则从反应开始到20min时,以H2表示的平均反应速率=__ mol/(L·min),该温度下平衡常数k=__ 。
③若在恒温恒压条件下进行上述反应,达到平衡后,往体系中通入一定量的稀释剂(水蒸气),CO的转化率__ (填"增大"、"减小"或"不变")。
(3)现在容积均为1L的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是__ 。达到平衡时,a、b、c中CO的转化率大小关系为__ 。

(1)已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(2)某研究性学习小组在容积固定为2L的密闭容器内充入1molCO和2molH2,加入合适催化剂(体积可以忽略不计)后进行反应CO(g)+2H2(g)=CH3OH(g) ΔH<0。
①下列措施中有利于增大该反应的反应速率且提高转化率的是
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.使用高效催化剂 D.增大体系压强
②实验过程中用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
则从反应开始到20min时,以H2表示的平均反应速率=
③若在恒温恒压条件下进行上述反应,达到平衡后,往体系中通入一定量的稀释剂(水蒸气),CO的转化率
(3)现在容积均为1L的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


