填空题 困难0.15 引用1 组卷529
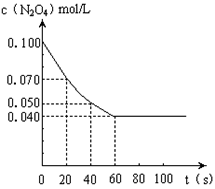
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4 2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
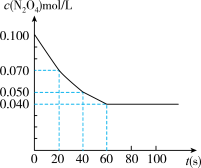
(1)计算在20至40秒时间内,NO2的平均生成速率为________ 。
(2)该反应的化学平衡常数表达式为_____________ 。
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
据此可推测该反应(生成NO2)是_______ 反应(选填“吸热”或“放热”)。
(4)若其他条件不变,反应在423K时达到平衡,请在上图中找出相应的位置,画出此温度下的反应进程示意曲线。
 2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)计算在20至40秒时间内,NO2的平均生成速率为
(2)该反应的化学平衡常数表达式为
(3)下表是不同温度下测定得到的该反应的化学平衡常数。
| T/ K | 323 | 373 |
| K值 | 0.022 | 0.36 |
据此可推测该反应(生成NO2)是
(4)若其他条件不变,反应在423K时达到平衡,请在上图中找出相应的位置,画出此温度下的反应进程示意曲线。
14-15高二下·福建泉州·期中
类题推荐
在温度为370 ℃时,将0.100 mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4⇌2NO2的平衡。下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
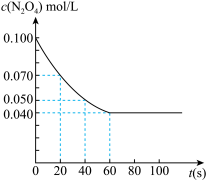
(1)20s至40s内v(N2O4)为_______ mol•L-1•s -1 。
(2)反应到达平衡时,N2O4的平衡转化率为_______ 。
(3)请计算该反应的化学平衡常数_______ 。
(4)表是不同温度下测定得到的该反应的化学平衡常数。
据此可推测该反应(生成NO2)是_______ 反应(选填“吸热”或“放热”)。
(5)该反应是否达到化学平衡状态的依据是_______ 。
a.容器中压强不变 b.混合气体中 c(NO2)不变
c.v正(N2O4)=v逆(NO2) d.c(NO2)=c(N2O4)

(1)20s至40s内v(N2O4)为
(2)反应到达平衡时,N2O4的平衡转化率为
(3)请计算该反应的化学平衡常数
(4)表是不同温度下测定得到的该反应的化学平衡常数。
| T/ K | 320℃ | 330℃ |
| K值 | 0.022 | 0.26 |
(5)该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中 c(NO2)不变
c.v正(N2O4)=v逆(NO2) d.c(NO2)=c(N2O4)
在100 ℃时,将0.40 mol二氧化氮气体充入2 L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
⑴在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为_________ mol/(L·min)。
⑵此条件下该反应的化学平衡常数的值约为___________ (保留两位有效数字)。
⑶若达到平衡后,降低温度,气体颜色会变浅,则该反应的平衡常数将____________ (填“增大”、“减小”或“不变”)。
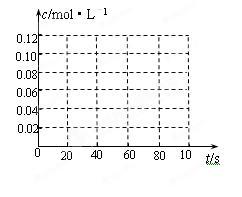
⑷若在相同情况下最初向该容器中充入的是N2O4气体,要达到初始数据表中同样的平衡状态,N2O4的起始浓度是_______________ ;假设在80 s时达到平衡,请在上图中画出并标明该条件下此反应中N2O4和NO2的浓度随时间变化的曲线。_____________________
⑸计算⑷中条件下达到平衡后N2O4的转化率__________________ 。
时间(s) | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
⑴在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为
⑵此条件下该反应的化学平衡常数的值约为
⑶若达到平衡后,降低温度,气体颜色会变浅,则该反应的平衡常数将

⑷若在相同情况下最初向该容器中充入的是N2O4气体,要达到初始数据表中同样的平衡状态,N2O4的起始浓度是
⑸计算⑷中条件下达到平衡后N2O4的转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
2NO2的平衡.下图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)