解答题-实验探究题 较难0.4 引用1 组卷351
三颈瓶在化学实验中的应用非常广泛,下面是三颈瓶在部分无机实验或有机实验中的一些应用。
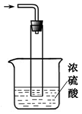
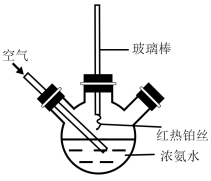
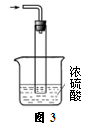
(1)在如图所示装置中,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中NH3∙H2O的电离程度____ (填“变大”、“变小”或“不变”)
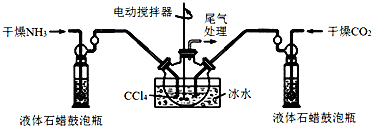
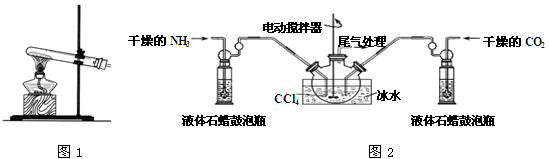
Ⅱ.实验室用下图所示装置制备氨基甲酸铵(NH2COONH4),其反应化学方程式:2NH3(g)+CO2(g) NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢铵。
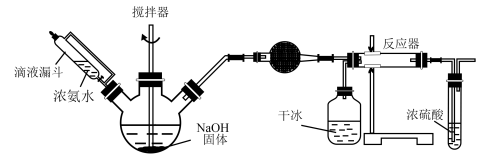
(2)写出加入药品之前实验操作的要点_______ ;反应中若有水存在则生成碳酸氢铵的化学方程式是________________________ 。
(3)干燥管中盛放的药品是______ 。简述左侧三颈瓶装置制取氨气的原理________ 。
(4)对比碳酸盐和酸的反应制取CO2,该实验利用干冰升华产生气体CO2的有优点有_____ .
(5)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是________ 。
(6)氨基甲酸氨可用作肥料,其肥效比尿素[CO(NH2)2]_______ (填“高”或“低”),在潮湿的空气中释放出氨而变成碳酸氢铵。取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7830g,用足量石灰水充分处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g,则样品中氨基甲酸铵的物质的量分数是_____________ 。
(1)在如图所示装置中,进行氨的催化氧化实验:向三颈瓶内的浓氨水中不断通入空气,将红热的铂丝插入瓶子并接近液面。反应过程中可观察到瓶中有红棕色气体产生,铂丝始终保持红热。实验过程中NH3∙H2O的电离程度

Ⅱ.实验室用下图所示装置制备氨基甲酸铵(NH2COONH4),其反应化学方程式:2NH3(g)+CO2(g)

(2)写出加入药品之前实验操作的要点
(3)干燥管中盛放的药品是
(4)对比碳酸盐和酸的反应制取CO2,该实验利用干冰升华产生气体CO2的有优点有
(5)有同学认为该实验装置存在安全问题,请问可能面临的安全问题是
(6)氨基甲酸氨可用作肥料,其肥效比尿素[CO(NH2)2]
14-15高三·新疆乌鲁木齐·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


 NH2COONH4(s)△H<0
NH2COONH4(s)△H<0