解答题-实验探究题 较难0.4 引用2 组卷575
氧化剂H2O2在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。
I.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
(1)实验①和②的目的是_________________________________ 。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是_________________________ (填一种方法即可)。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。
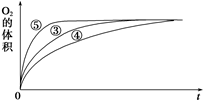
分析该图能够得出的实验结论是________________________________ 。
II.资料显示,某些金属离子或金属氧化物对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如下图所示的实验装置进行实验。
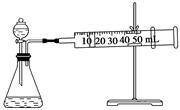
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量_______ 或______ 来比较。
(2)0.1 g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。请解释化学反应速率变化的原因:_____________ 。请计算H2O2的初始物质的量浓度为________________ (保留两位有效数字)。
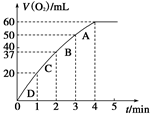
为探究MnO2在此实验中对H2O2的分解起催化作用,需补做下列实验(无 需写出具体操作):a._________________ ;b.___________________ 。
I.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析该图能够得出的实验结论是
II.资料显示,某些金属离子或金属氧化物对H2O2的分解起催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,该实验小组的同学设计了如下图所示的实验装置进行实验。

(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量
(2)0.1 g MnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。请解释化学反应速率变化的原因:

为探究MnO2在此实验中对H2O2的分解起催化作用,需补做下列实验(无 需写出具体操作):a.
2015·广东揭阳·二模
类题推荐
氧化剂H2O2在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。
I.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
(1)实验①和②的目的是探究________对反应速率的影响。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析该图能够得出的实验结论是___________。
II.资料显示,某些金属离子对H2O2的分解起催化作用。为探究不同浓度的Fe3+对H2O2分解的催化效果,实验小组的同学设计了如下图所示的实验装置进行实验。
限选试剂:30% H2O2、0.1mol∙L-1Fe2(SO4)3、蒸馏水
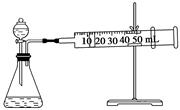
(3)某同学通过测定O2的体积来比较H2O2的分解速率快慢。实验时可以通过测量_________来比较。(要求所测得的数据能直接体现反应速率大小)。
(4)参照下表格式,拟定实验表格,完整体现上述实验的方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示)。
I.某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
| 实验编号 | 反应物 | 加入物质 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 9 mL 5% H2O2溶液 | 1 mL 水 |
| ④ | 9 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 HCl溶液 |
| ⑤ | 9 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 NaOH溶液 |
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析该图能够得出的实验结论是___________。
II.资料显示,某些金属离子对H2O2的分解起催化作用。为探究不同浓度的Fe3+对H2O2分解的催化效果,实验小组的同学设计了如下图所示的实验装置进行实验。
限选试剂:30% H2O2、0.1mol∙L-1Fe2(SO4)3、蒸馏水

(3)某同学通过测定O2的体积来比较H2O2的分解速率快慢。实验时可以通过测量_________来比较。(要求所测得的数据能直接体现反应速率大小)。
(4)参照下表格式,拟定实验表格,完整体现上述实验的方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示)。
| 物理量 实验序号 | V[30% H2O2]/mL | …… | |
| 1 | a | …… | |
| 2 | a | …… |
某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下表所示的方案完成实验。
(1)实验①和②的目的是__________ 。同学们进行实验时没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进方法是_________ (填一种方法即可)。
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。
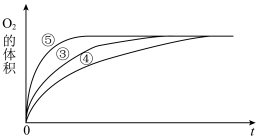
分析该图能够得出的实验结论是___________ 。
| 实验编号 | 反应物 | 催化剂 |
| ① | 10 mL 2% H2O2溶液 | 无 |
| ② | 10 mL 5% H2O2溶液 | 无 |
| ③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
| ⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
(1)实验①和②的目的是
(2)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析该图能够得出的实验结论是
氧化剂H2O2在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验小组以H2O2分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成实验。
(1)实验①和②的目的是___________ 。甲同学在进行实验时并没有观察到明显现象。资料显示,通常条件下过氧化氢稳定,不易分解。为了达到实验目的,可采取的改进方法是___________ (写出一种即可)。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。由图可知⑤中温度t___________ 20℃(填“>”、“<”或“=”),分析该图能得出的结论是___________ 对H2O2分解的催化效果更好。

(3)写出实验③中H2O2分解的化学方程式:___________ ,催化剂能增大化学反应速率的原因是___________ 。
(4)乙同学设计了乙图所示的实验装置对H2O2的分解速率进行定量分析。以生成10mL气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是___________ 。

| 实验编号 | 温度(℃) | 反应物 | 催化剂 |
| ① | 20 | 25 mL 3% H2O2溶液 | 无 |
| ② | 20 | 25 mL 5% H2O2溶液 | 无 |
| ③ | 20 | 25 mL 5% H2O2溶液 | 0.1g MnO2 |
| ④ | 20 | 25 mL 5% H2O2溶液 | 1~2滴1mol/L FeCl3溶液 |
| ⑤ | t | 25 mL 5% H2O2溶液 | 0.1g MnO2 |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。由图可知⑤中温度t

(3)写出实验③中H2O2分解的化学方程式:
(4)乙同学设计了乙图所示的实验装置对H2O2的分解速率进行定量分析。以生成10mL气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


