解答题-实验探究题 困难0.15 引用2 组卷1082
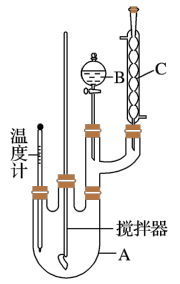
实验室制备硝基苯的反应原理和实验装置如下:
有关数据列如下表
取100mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)装置B的名称是_______________ 。装置C的作用是_________________________ 。
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:________________ 。
(3)为了使反应在50℃~60℃下进行,常用的方法是______________________ 。
(4)在洗涤操作中,第二次水洗的作用是__________________________ 。
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是_____________________________________________ 。
(6)本实验所得到的硝基苯产率是____________________________________ 。
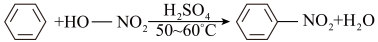 ΔH<0
ΔH<0
有关数据列如下表
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
取100mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混和酸,将混合酸小心加入B中。把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
(1)装置B的名称是
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:
(3)为了使反应在50℃~60℃下进行,常用的方法是
(4)在洗涤操作中,第二次水洗的作用是
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是
(6)本实验所得到的硝基苯产率是
14-15高三·河南洛阳·阶段练习
类题推荐
某科学研究小组制备硝基苯的实验装置如图所示,相关数据见下表。已知该实验中存在的主要副反应是:在温度稍高的情况下会生成间二硝基苯。

实验步骤如下:
取 浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心加入
浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心加入 中。取
中。取 (
( )苯加入
)苯加入 中。在室温下,向苯中逐滴加入混合酸,边滴加边搅拌,混合均匀加热,使其在50~60℃下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、
中。在室温下,向苯中逐滴加入混合酸,边滴加边搅拌,混合均匀加热,使其在50~60℃下发生反应,直至反应结束。将反应液冷却至室温后倒入分液漏斗中,依次用少量水、 溶液和水洗涤。在分出的产物中加入无水
溶液和水洗涤。在分出的产物中加入无水 颗粒,静置片刻,过滤,对滤液进行蒸馏纯化,收集
颗粒,静置片刻,过滤,对滤液进行蒸馏纯化,收集 的馏分,得到纯硝基苯
的馏分,得到纯硝基苯 。
。
回答下列问题:
(1)图中装置 的作用是
的作用是___________ 。
(2)制备硝基苯的化学方程式为___________ 。
(3)配制混合酸时,能否将浓硝酸加入浓硫酸中?___________ (填“能”或“不能”),说明理由:___________ 。
(4)为了使反应在 下进行,常采用的加热方法是
下进行,常采用的加热方法是___________ 。反应结束并冷却至室温后 中液体为粗硝基苯,粗硝基苯呈黄色的原因是
中液体为粗硝基苯,粗硝基苯呈黄色的原因是___________ 。
(5)在洗涤操作中,第二次水洗的目的是___________ 。
(6)本实验所得到的硝基苯的产率是___________ 。
| 物质 | 熔点 | 沸点 | 密度 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 不溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | -42 | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | 10.4 | 338 | 1.84 | 易溶于水 |

实验步骤如下:
取
回答下列问题:
(1)图中装置
(2)制备硝基苯的化学方程式为
(3)配制混合酸时,能否将浓硝酸加入浓硫酸中?
(4)为了使反应在
(5)在洗涤操作中,第二次水洗的目的是
(6)本实验所得到的硝基苯的产率是
某科研小组制备硝基苯的实验装置如下,有关数据如下表:
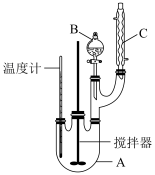
实验步骤如下:
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心地加入B中。把15.6g苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混合均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水 颗粒,静置片刻,弃去
颗粒,静置片刻,弃去 ,然后进一步提纯得到纯硝基苯17.22g。
,然后进一步提纯得到纯硝基苯17.22g。
回答下列问题:
(1)装置中仪器C的名称是_______ ;为了使反应在50~60℃下进行,常用的加热方式是_______ 。
(2)将粗产品置于分液漏斗中加水,振荡后静置,产物应在_______ (填“上”或“下”)层,在洗涤操作中,第二次水洗的作用是_______ 。
(3)步骤中加入无水 的目的是
的目的是_______ ,进一步提纯采用的操作方法为_______ 。
(4)本实验所得到的硝基苯的产率为_______ 。
| 物质 | 熔点/℃ | 沸点/℃ | 密度 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 不溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硫酸 | - | 338 | 1.84 | 易溶于水 |

实验步骤如下:
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混合酸,将混合酸小心地加入B中。把15.6g苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混合均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水
回答下列问题:
(1)装置中仪器C的名称是
(2)将粗产品置于分液漏斗中加水,振荡后静置,产物应在
(3)步骤中加入无水
(4)本实验所得到的硝基苯的产率为
I、实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:完成下列问题:

(1)不能用铁丝搅拌棒代替环形玻璃搅拌棒的理由是_______
(2)经数据处理,测得中和热为56.8 kJ·mol-1其热化学方程式为:___________
II.实验室制备硝基苯实验装置和步骤如下:(实验步骤)

取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝基苯18.00 g。请回答:
(1)装置B的名称是________ ,装置C的作用是________________ 。
(2)实验室制备硝基苯的化学方程式是____________________________ 。
(3)为了使反应在50~60 ℃下进行,常用的方法是__________ 。
(4)在洗涤操作中,第二次水洗的作用是____________________ 。
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |

(1)不能用铁丝搅拌棒代替环形玻璃搅拌棒的理由是
(2)经数据处理,测得中和热为56.8 kJ·mol-1其热化学方程式为:
II.实验室制备硝基苯实验装置和步骤如下:(实验步骤)

取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝基苯18.00 g。请回答:
(1)装置B的名称是
(2)实验室制备硝基苯的化学方程式是
(3)为了使反应在50~60 ℃下进行,常用的方法是
(4)在洗涤操作中,第二次水洗的作用是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


