解答题-工业流程题 适中0.65 引用2 组卷614
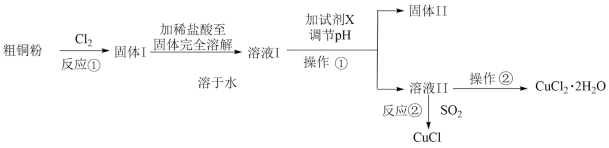
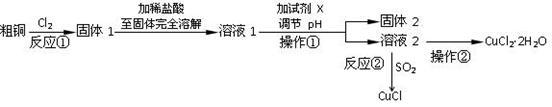
过渡金属的单质及化合物很多有催化性能,氯化铜、氯化亚铜经常用作有机合成催化剂。实验室中用氯气与粗铜(杂质只有Fe)反应,制备铜的氯化物的流程如下。

查阅资料:
氯化亚铜:白色微溶于水,在干燥空气中稳定,受潮则易变蓝到棕色,在热水中迅速水解生成氧化铜水合物而呈红色。
氯化铜:从水溶液中结晶时,在26~42℃得到二水物,在15℃以下得到四水物,在15~25.7℃得到三水物,在42℃以上得到一水物,在100℃得到无水物。
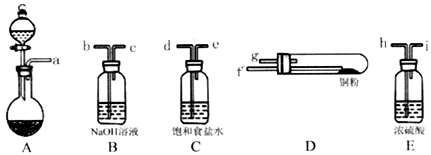
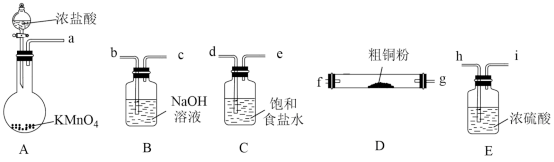
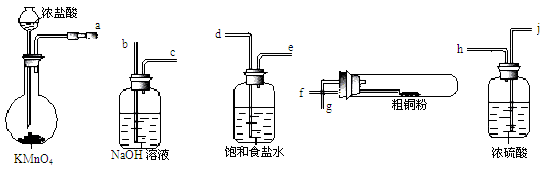
(1)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。
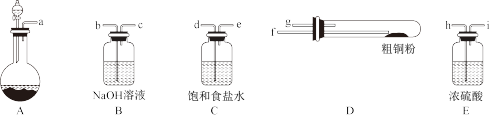
①按气流方向连接各仪器接口顺序是:a→___ 、___ → h 、i →___ 、___ →___ 。
②本套装置有两个仪器需要加热,加热的顺序为先___ 后___ ,这样做的目的是___ 。
(2)分析流程:
①固体甲需要加稀盐酸溶解,其理由是___ ;
②溶液甲可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)___ 。
a.NaOH b. NH3·H2O c.CuO d.CuSO4
③完成溶液乙到纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、___ 、___ 、洗涤、干燥。
(3)向溶液乙中加入适当的还原剂(如SO2、N2H4、SnCl2等),并微热得到CuCl沉淀,写出向乙溶液加入N2H4(氧化产物为无毒气体)的离子方程式:___ 。此反应只能微热的原因是___ 。
(4)若开始取100g 含铜96%的粗铜与足量Cl2反应,经上述流程只制备CuCl2·2H2O,最终得到干燥产品277g,求制备CuCl2·2H2O的产率___ ;(精确到1%)分析出现此情况的主要原因______ 。

查阅资料:
氯化亚铜:白色微溶于水,在干燥空气中稳定,受潮则易变蓝到棕色,在热水中迅速水解生成氧化铜水合物而呈红色。
氯化铜:从水溶液中结晶时,在26~42℃得到二水物,在15℃以下得到四水物,在15~25.7℃得到三水物,在42℃以上得到一水物,在100℃得到无水物。
(1)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。

①按气流方向连接各仪器接口顺序是:a→
②本套装置有两个仪器需要加热,加热的顺序为先
(2)分析流程:
①固体甲需要加稀盐酸溶解,其理由是
②溶液甲可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号)
a.NaOH b. NH3·H2O c.CuO d.CuSO4
③完成溶液乙到纯净CuCl2·2H2O晶体的系列操作步骤为:加少量盐酸、蒸发浓缩、
(3)向溶液乙中加入适当的还原剂(如SO2、N2H4、SnCl2等),并微热得到CuCl沉淀,写出向乙溶液加入N2H4(氧化产物为无毒气体)的离子方程式:
(4)若开始取100g 含铜96%的粗铜与足量Cl2反应,经上述流程只制备CuCl2·2H2O,最终得到干燥产品277g,求制备CuCl2·2H2O的产率
2015·浙江温州·一模
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网