解答题-原理综合题 适中0.65 引用1 组卷475
研究碳、氮氧化物的性质与利用具有重要意义。
(1)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是________ 。
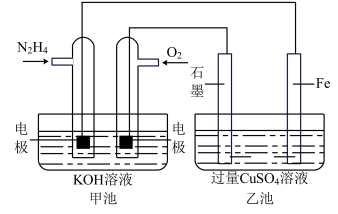
②由MgO制成的Mg可构成“镁——次氯酸盐”电池,其装置示意图如图1,该电池的正极反应式为_________________ ;
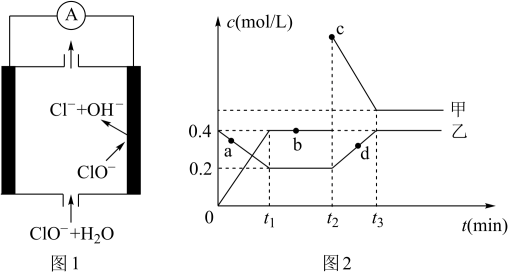
(2)化合物甲、乙是两种氮的氧化物且所含元素价态均相同,某温度下相互转化时的量变关系如图2所示:
①甲的化学式是_______________ ;
②图中a、b、c、d四点中,表示反应处于平衡状态的是_________ 。t1~t2时间内v正(乙)_____ v逆(甲)(填“>”“<”或“=”)
③反应进行到t2时刻,改变的条件可能是_____________ 。
(3)用H2或CO催化还原NO可达到消除污染的目的。
已知:2NO(g) = N2(g) + O2(g) △H = -180.5kJ·mol-1
2H2O(l) = 2H2(g) + O2(g) △H = +571.6kJ·mol-1
则用H2催化还原NO消除污染的热化学方程式是__________________ 。
(1)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量的SO2和SO3,此时反应的化学方程式是
②由MgO制成的Mg可构成“镁——次氯酸盐”电池,其装置示意图如图1,该电池的正极反应式为

(2)化合物甲、乙是两种氮的氧化物且所含元素价态均相同,某温度下相互转化时的量变关系如图2所示:
①甲的化学式是
②图中a、b、c、d四点中,表示反应处于平衡状态的是
③反应进行到t2时刻,改变的条件可能是
(3)用H2或CO催化还原NO可达到消除污染的目的。
已知:2NO(g) = N2(g) + O2(g) △H = -180.5kJ·mol-1
2H2O(l) = 2H2(g) + O2(g) △H = +571.6kJ·mol-1
则用H2催化还原NO消除污染的热化学方程式是
14-15高三·福建福州·阶段练习
类题推荐
Ⅰ.制水煤气的主要化学反应方程式为:C(s)+H2O(g) CO(g)+H2(g),此反应是吸热反应。
CO(g)+H2(g),此反应是吸热反应。
①此反应的化学平衡常数表达式为____________________ ;
②下列能提高碳的平衡转化率的措施是____________________ 。
E.将碳研成粉末
Ⅱ.研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)已知石墨的标准燃烧热为y kJ·mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量。则石墨与氧气反应生成CO的热化学方程式为:
________________________________________________________________ 。
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是:
________________________________________________________________ 。
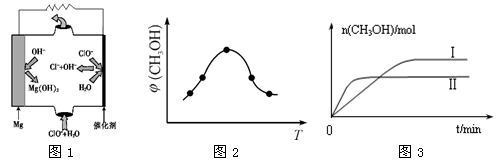
②由MgO可制成“镁—次氯酸盐”燃料电池,其装置示意图如图1所示,该电池反应的离子方程式为:_____________________________________________________________ 。
(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH__________ (填“>” “<”或“=”)0。
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ 对应的平衡常数大小关系为KⅠ__________________ KⅡ(填“>” “<”或“=”)。
③一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为____________________ 。
①此反应的化学平衡常数表达式为
②下列能提高碳的平衡转化率的措施是
| A.加入C(s) |
| B.加入H2O(g) |
| C.升高温度 |
| D.增大压强 |
E.将碳研成粉末
Ⅱ.研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)已知石墨的标准燃烧热为y kJ·mol-1,1.2g石墨在1.68L(标准状况)氧气中燃烧,至反应物耗尽,放出x kJ热量。则石墨与氧气反应生成CO的热化学方程式为:
(2)高温时,用CO还原MgSO4可制备高纯MgO。
①750℃时,测得气体中含等物质的量SO2和SO3,此时反应的化学方程式是:
②由MgO可制成“镁—次氯酸盐”燃料电池,其装置示意图如图1所示,该电池反应的离子方程式为:

(3)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g)
①取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图2所示,则上述CO2转化为甲醇反应的ΔH
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图3所示,曲线I、Ⅱ 对应的平衡常数大小关系为KⅠ
③一定温度下,在容积相同且固定的两个密闭容器中,按如下方式投入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2 3molH2 | a molCO2、b molH2、 c molCH3OH(g)、c molH2O(g) |
若甲中平衡后气体的压强为开始时的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持反应逆向进行,则c的取值范围为
NO2、NO、CO等是常见大气污染物,研究NO2、NO、CO等污染物的处理对建设美丽中国具有重要的意义。
(1)已知:①NO2(g)+CO(g)⇌CO2(g)+NO(g),断开1mol下列物质的所有化学键时所消耗能量分别为:
② N2(g)+
N2(g)+ O2(g)⇌NO(g)ΔH=+89.75kJ·mol-1
O2(g)⇌NO(g)ΔH=+89.75kJ·mol-1
③2NO(g)+O2(g)⇌2NO2(g)ΔH=-112.3kJ·mol-1
写出NO与CO反应生成无污染气体的热化学方程式:__ 。
(2)污染性气体NO2与CO在一定条件下的反应为2NO2(g)+4CO(g)⇌4CO2(g)+N2(g),某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1atm,5s时反应达到平衡,容器的压强变为原来的 ,则反应开始到平衡时CO的平均反应速率为ν(CO)=
,则反应开始到平衡时CO的平均反应速率为ν(CO)=_ ;若此温度下,某时刻测得NO2、CO、CO2、N2的浓度分别为amol·L-1、0.4mol·L-1、0.1mol·L-1、1mol·L-1,要使反应向逆反应方向进行,a的取值范围为__ 。
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)ΔH<0.现在向体积为2L的恒容密闭容器(如图甲所示)中通入1molCO和2molH2:

测定不同时刻、不同温度(T/℃)下容器中CO的物质的量如下表:
请回答:
①T1__ (填“>”或“<”或“=”)T2,理由是__ 。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为___ ,该温度下的化学平衡常数为___ 。
②若将1molCO和2molH2通入原体积为2L的恒压密闭容器(如图乙所示)中,达平衡后再向容器中通入1molCH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量___ 。
(填“变大”、“变小”或“不变”)。
(1)已知:①NO2(g)+CO(g)⇌CO2(g)+NO(g),断开1mol下列物质的所有化学键时所消耗能量分别为:
| NO2 | CO | CO2 | NO |
| 812kJ | 1076kJ | 1490kJ | 632kJ |
③2NO(g)+O2(g)⇌2NO2(g)ΔH=-112.3kJ·mol-1
写出NO与CO反应生成无污染气体的热化学方程式:
(2)污染性气体NO2与CO在一定条件下的反应为2NO2(g)+4CO(g)⇌4CO2(g)+N2(g),某温度下,在1L密闭容器中充入0.1molNO2和0.2molCO,此时容器的压强为1atm,5s时反应达到平衡,容器的压强变为原来的
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)ΔH<0.现在向体积为2L的恒容密闭容器(如图甲所示)中通入1molCO和2molH2:

测定不同时刻、不同温度(T/℃)下容器中CO的物质的量如下表:
| 温度 | 不同时刻容器中CO的物质的量 | ||||
| 0min | 10min | 20min | 30min | 40min | |
| T1 | 1mol | 0.8mol | 0.62mol | 0.4mol | 0.4mol |
| T2 | 1mol | 0.7mol | 0.5mol | a | a |
①T1
②若将1molCO和2molH2通入原体积为2L的恒压密闭容器(如图乙所示)中,达平衡后再向容器中通入1molCH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量
(填“变大”、“变小”或“不变”)。
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网