填空题 适中0.64 引用4 组卷214
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是________ 、________ 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?______ (填“能”或“否”),
(3)他们记录的实验数据如下:
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
①根据实验数据计算并写出NaOH溶液与HCl溶液反应的热化学方程式:_______________
(4)若用KOH代替NaOH,对测定结果____ (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果_____ (填“有”或“无”)影响。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol· L-1 盐酸、0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?
(3)他们记录的实验数据如下:
| 实 验 用 品 | 溶 液 温 度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.3℃ | |
| ② | 50mL0.55mol.L-1NaOH | 50mL.0.5mol.L-1HCl | 20℃ | 23.5℃ | |
已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18KJ·℃-1· kg-1,各物质的密度均为1g·cm-3。
①根据实验数据计算并写出NaOH溶液与HCl溶液反应的热化学方程式:
(4)若用KOH代替NaOH,对测定结果
14-15高二上·云南玉溪·期中
类题推荐
某化学兴趣小组要完成中和反应反应热的测定实验。
(1)实验桌上备有量热计、胶头滴管、玻璃搅拌器、 盐酸、
盐酸、 氢氧化钠溶液,实验尚缺少的玻璃用品是
氢氧化钠溶液,实验尚缺少的玻璃用品是_______ 。
(2)实验中能否用环形铜丝搅拌器代替玻璃搅拌器_______ (填“能”或“否”),其原因是_______ 。
(3)他们记录的实验数据如下:
已知: ,反应后溶液的比热容c为
,反应后溶液的比热容c为 ,各物质的密度均为
,各物质的密度均为 。
。
①计算完成上表(保留1位小数)_______ 。
②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:_______ 。
(4)若用氢氧化钾代替氢氧化钠,对测定结果_______ (填“有”或“无”,下同)影响;若用醋酸代替盐酸做实验,对测定结果_______ 影响。
(1)实验桌上备有量热计、胶头滴管、玻璃搅拌器、
(2)实验中能否用环形铜丝搅拌器代替玻璃搅拌器
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 生成 | |||
| a | 20℃ | 23.3℃ | _______kJ | ||
| b | 20℃ | 23.5℃ | |||
①计算完成上表(保留1位小数)
②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:
(4)若用氢氧化钾代替氢氧化钠,对测定结果
某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol·L-1盐酸、0.55mol·L-1NaOH溶液,尚缺少的实验玻璃用品是______________ 、_________________ 。
(2)他们记录的实验数据如下:
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18kJ·℃-1·kg-1,各物质的密度均为lg·cm-3。计算完成上表。△H=____________
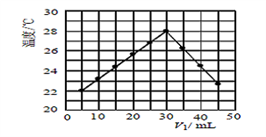
(3)某研究小组将V1mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2 =50mL)。此反应所用NaOH溶液的浓度应为__________ mol/L。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol·L-1盐酸、0.55mol·L-1NaOH溶液,尚缺少的实验玻璃用品是
| 实验用品 | 溶液温度 | 中和热△H | |||
| t1 | t2 | ||||
| ① | 50mL0.55mol·L-1NaOH | 50mL.0.5mol·L-1HCl | 20℃ | 23.3℃ | _______ |
| ② | 50mL0.55mol·L-1NaOH | 50mL.0.5mol·L-1HCl | 20℃ | 23.5℃ | |
(2)他们记录的实验数据如下:
已知:Q=Cm(t2-t1),反应后溶液的比热容C为4.18kJ·℃-1·kg-1,各物质的密度均为lg·cm-3。计算完成上表。△H=
(3)某研究小组将V1mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2 =50mL)。此反应所用NaOH溶液的浓度应为

某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、50mL量筒两个,0.55mol·L-1NaOH溶液、0.50mol·L-1盐酸,实验尚缺少的玻璃仪器是__ 。
(2)他们记录的实验数据如下:(t1为起始终止温度,t2为终止温度)
已知:Q=cmΔt,c为4.18J·℃-1·g-1,各溶液的密度均为1g·cm-3。
①通过计算得到中和热ΔH=___ kJ/mol(只列出计算式不计算结果)。
②根据①的计算式计算出中和热的数值为55.2,写出NaOH溶液与HCl溶液反应的热化学方程式:___ 。
(3)若用0.50mol·L-1醋酸代替0.50mol·L-1盐酸做实验,对测定结果___ 影响(填“有”或“无”)。
(4)本次实验测定值与正确值57.3kJ/mol有偏差,产生偏差的原因可能是___ (填序号)操作。
①量取NaOH溶液的体积时仰视读数
②用温度计测定NaOH溶液的温度后直接测定盐酸的温度
③分多次把NaOH溶液倒入装盐酸的小烧杯中
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、50mL量筒两个,0.55mol·L-1NaOH溶液、0.50mol·L-1盐酸,实验尚缺少的玻璃仪器是
(2)他们记录的实验数据如下:(t1为起始终止温度,t2为终止温度)
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | ΔH | |||
| ① | 50mL 0.55mol·L-1 NaOH溶液 | 50mL 0.50mol·L-1 HCl溶液 | 20℃ | 23.2℃ | |
| ② | 50mL 0.55mol·L-1 NaOH溶液 | 50mL 0.50mol·L-1 HCl溶液 | 20℃ | 23.4℃ | |
①通过计算得到中和热ΔH=
②根据①的计算式计算出中和热的数值为55.2,写出NaOH溶液与HCl溶液反应的热化学方程式:
(3)若用0.50mol·L-1醋酸代替0.50mol·L-1盐酸做实验,对测定结果
(4)本次实验测定值与正确值57.3kJ/mol有偏差,产生偏差的原因可能是
①量取NaOH溶液的体积时仰视读数
②用温度计测定NaOH溶液的温度后直接测定盐酸的温度
③分多次把NaOH溶液倒入装盐酸的小烧杯中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


