解答题-原理综合题 较难0.4 引用2 组卷376
道路千万条,安全第一条。当汽车在高速行驶中受到猛烈撞击时,会产生大量气体充满气囊,从而保护驾驶员和乘客的安全。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:______ (填“吸热”或“放热”)反应。
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为______ kJ(用含a、b的代数式表示)。
Ⅱ.汽车尾气中的 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:
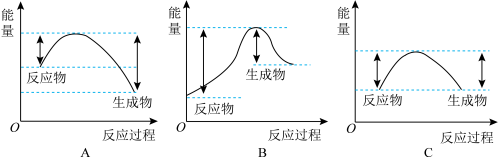
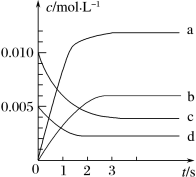
(3)下图表示 的变化的曲线是
的变化的曲线是______ ______ (选填序号,下同)。
a.容器内气体的颜色不再变化 b.
c. d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是______ 。
a.增大 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体
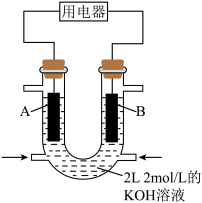
Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示:______ 极(填写“正”或“负”),M处电极反应式是______ ;
(7)该电池产生11.2L(标况下) ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为______ 。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:
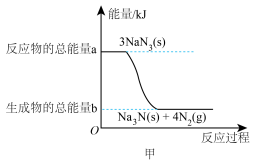
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为
Ⅱ.汽车尾气中的
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(3)下图表示
a.容器内气体的颜色不再变化 b.
c.
(5)为使该反应的反应速率增大,下列措施正确的是
a.增大
Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应
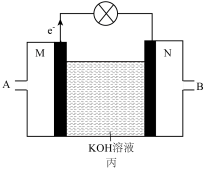
(7)该电池产生11.2L(标况下)
23-24高一下·福建·期中
类题推荐
I.减少交通事故除遵守交通法规正确驾驶外,安全措施也极为重要。汽车的安全气嚢内有叠氮化钠(NaN3)与硝酸铵(NH4NO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生分解反应,产生大量气体,充满气囊,从而保护驾驶员和乘客的安全。
请回答下列问题:
(1)下列判断正确的是_______
(2)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:_______ (填“吸热”或“放热”)反应。
②若爆炸过程中有18mol 非极性键生成(一个共用电子对为一个化学键),则反应的能量变化为______ kJ,消耗叠氮化钠的质量为_________ g。
③若安全气嚢的体积为VL,NaN3的爆炸在ts内完成,反应过程中消耗292.5g NaN3,则用N2表示的反应速率为____________ 。
II.已知X、Y、Z、W分别是元素周期表中的短周期元素,且原子序数依次增大。X、W为同主族元素,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中含有3个共价键,X、Y、Z所形成的常见化合物是汽车安全气囊中的一种填充物。请回答下列问题:
(3)①写出X、Y、W形成化合物的电子式___________ 。
②一定温度下,X2、Y2在容积为5L的密闭容器中发生可逆反应,充入的X2和Y2的物质的量分别是6mol和3mol,达到化学平衡状态时生成物的物质的量为2.4mol。达到化学平衡状态时,混合气体中Y2的体积分数为_________ 。
请回答下列问题:
(1)下列判断正确的是_______
| A.道路起雾与H2O分子的化学键断裂有关 |
| B.NH4NO3中只含有极性共价键 |
| C.NaN3受到猛烈撞击时化学键一定断裂 |
| D.NaN3、NH4NO3均属于离子化合物 |
(2)汽车的安全气囊内叠氮化钠爆炸过程中的能量变化如图所示:
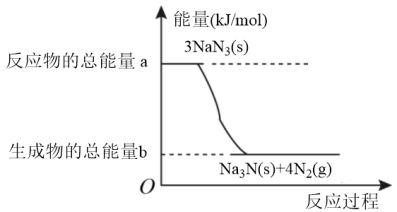
②若爆炸过程中有18mol 非极性键生成(一个共用电子对为一个化学键),则反应的能量变化为
③若安全气嚢的体积为VL,NaN3的爆炸在ts内完成,反应过程中消耗292.5g NaN3,则用N2表示的反应速率为
II.已知X、Y、Z、W分别是元素周期表中的短周期元素,且原子序数依次增大。X、W为同主族元素,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中含有3个共价键,X、Y、Z所形成的常见化合物是汽车安全气囊中的一种填充物。请回答下列问题:
(3)①写出X、Y、W形成化合物的电子式
②一定温度下,X2、Y2在容积为5L的密闭容器中发生可逆反应,充入的X2和Y2的物质的量分别是6mol和3mol,达到化学平衡状态时生成物的物质的量为2.4mol。达到化学平衡状态时,混合气体中Y2的体积分数为
CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
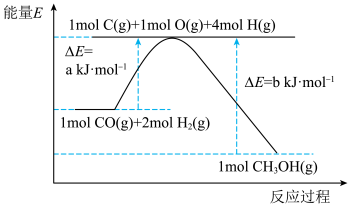
(1)已知利用合成气(主要成分CO和H2)在催化剂的作用下合成甲醇,发生反应为:CO(g)+2H2 (g) CH3OH(g)。反应过程中的能量变化如图所示,该反应为
CH3OH(g)。反应过程中的能量变化如图所示,该反应为___________ (填“放热”或“吸热”)反应。
(2)现在实验室中用CO和H2反应模拟甲醇合成反应,在2L恒容密闭容器内,400℃时发生反应:CO(g)+2H2 (g) CH3OH (g),体系中n(CO)随时间的变化如表:
CH3OH (g),体系中n(CO)随时间的变化如表:
①0~2min内,以H2表示的该反应速率v(H2)=___________  ;
;
②下列措施不能提高反应速率的有___________ (请用相应字母填空);
a.升高温度 b.恒T、恒V下充入H2
c.及时分离出CH3OH d.恒T、恒P下充入N2
e.加入高效催化剂
③下列叙述能说明反应达到平衡状态的是___________ (请用相应字母填空);
a.CO和H2的浓度保持不变 b. 2v正(H2)=v逆(CO)
c.容器内气体密度保持不变 d.容器内质量保持不变
e.每生成1mol CH3OH的同时有2mol H-H键形成
(3)化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H2SO4溶液作电解质溶液,其简易装置如图所示。
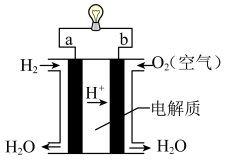
在这个燃料电池中,正极的电极反应式为_______________________ 。若在标况下,消耗了33.6L的氢气,此时电路中转移的电子数目为______________ (用阿伏加德罗常数表示)。
(1)已知利用合成气(主要成分CO和H2)在催化剂的作用下合成甲醇,发生反应为:CO(g)+2H2 (g)

(2)现在实验室中用CO和H2反应模拟甲醇合成反应,在2L恒容密闭容器内,400℃时发生反应:CO(g)+2H2 (g)
时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO) (mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
②下列措施不能提高反应速率的有
a.升高温度 b.恒T、恒V下充入H2
c.及时分离出CH3OH d.恒T、恒P下充入N2
e.加入高效催化剂
③下列叙述能说明反应达到平衡状态的是
a.CO和H2的浓度保持不变 b. 2v正(H2)=v逆(CO)
c.容器内气体密度保持不变 d.容器内质量保持不变
e.每生成1mol CH3OH的同时有2mol H-H键形成
(3)化学能与其他能量间的转换在生活中处处可见,比如某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H2SO4溶液作电解质溶液,其简易装置如图所示。

在这个燃料电池中,正极的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网