解答题-结构与性质 适中0.65 引用1 组卷57
碳、硅元素及其化合物在生产生活中应用广泛。请回答:
(1)基态硅原子核外电子排布式:_______ 。该基态原子占据最高能级的电子云轮廓图形状为_______ 。
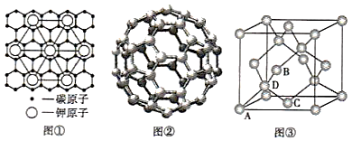
(2)C60晶体采用面心立方堆积,C60晶体中存在的作用力有_______ (填字母)
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键 F.金属键
(3)与碳的氢化物类似,硅元素的氢化物硅烷的通式为:SinH2n+2。下列有关说法不正确的是_______。
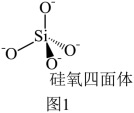
(4)硅酸盐是地壳中的主要成分。硅酸盐的最简单阴离子为SiO ,为硅氧四面体,结构如图1。SiO
,为硅氧四面体,结构如图1。SiO 在溶液中形成的分子形态脱水易形成凝胶状的固体物质—硅胶。硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架—SiO2(硅石)。联系相关信息,解释硅胶转变为硅石后,硬度变大的原因:
在溶液中形成的分子形态脱水易形成凝胶状的固体物质—硅胶。硅胶继续脱水,形成了共用氧原子的硅氧四面体骨架—SiO2(硅石)。联系相关信息,解释硅胶转变为硅石后,硬度变大的原因:_______ 。 ,KCx晶胞结构如图2(碳原子省略),如图3是晶胞沿y轴方向的投影。
,KCx晶胞结构如图2(碳原子省略),如图3是晶胞沿y轴方向的投影。_______ 。
②若石墨层内的大π键可表示为 (上标表示电子总数,下标表示原子数),则平均每个KCx单元中的大π键可表示为
(上标表示电子总数,下标表示原子数),则平均每个KCx单元中的大π键可表示为_______ (用具体的数据表示)。
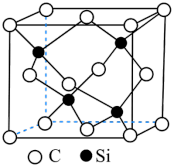
(6)已知 晶体的密度为ρg· cm-3,其晶胞结构如图所示。阿伏加德罗常数值为NA,则晶胞中两个
晶体的密度为ρg· cm-3,其晶胞结构如图所示。阿伏加德罗常数值为NA,则晶胞中两个 原子之间的距离为
原子之间的距离为_______  。
。
(1)基态硅原子核外电子排布式:
(2)C60晶体采用面心立方堆积,C60晶体中存在的作用力有
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键 F.金属键
(3)与碳的氢化物类似,硅元素的氢化物硅烷的通式为:SinH2n+2。下列有关说法不正确的是_______。
| A.Si3H8没有同分异构体 |
| B.Si-Si键能比C-C键能小,故热稳定性:SinH2n+2>CnH2n+2 |
| C.SinH2n+2中Si原子杂化方式均为sp3 |
| D.SinH2n+2可与水反应生成氢气 |

②若石墨层内的大π键可表示为
(6)已知
2024·宁夏银川·三模
类题推荐
硼、碳、氮、磷、硫等元素形成的单质和化合物在生活、生产中有重要的用途。
(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是___________ (填字母)。
A. B.
B.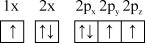
C.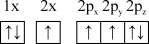 D.
D.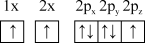
(2)氢、硼、碳、硫四元素的电负性由大到小的顺序为___________
(3)(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为___________ 。其σ键分别为___________ 型σ键。
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为___________

(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和对应金属阳离子的半径。随着金属阳离子半径的增大,碳酸盐的热分解温度逐渐升高,原因是___________
(6)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性 (晶体结构如图)。
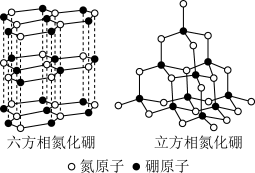
①关于这两种晶体的说法,不正确的是___________ (填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B﹣N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体其结构与石墨相似却不导电,原因是___________
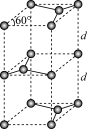
(7)石墨的晶胞结构如图所示。已知石墨的密度为ρg·cm-3,C-C键的键长为r cm,NA为阿伏加德罗常数的值,则石墨晶体的层间距d=___________ cm。
(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是
A.
 B.
B.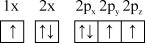
C.
 D.
D.
(2)氢、硼、碳、硫四元素的电负性由大到小的顺序为
(3)(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为

(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和对应金属阳离子的半径。随着金属阳离子半径的增大,碳酸盐的热分解温度逐渐升高,原因是
| 碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 402 | 900 | 1172 | 1360 |
| 金属阳离子半径/pm | 66 | 99 | 112 | 135 |

①关于这两种晶体的说法,不正确的是
a.两种晶体均为分子晶体
b.两种晶体中的B﹣N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体其结构与石墨相似却不导电,原因是
(7)石墨的晶胞结构如图所示。已知石墨的密度为ρg·cm-3,C-C键的键长为r cm,NA为阿伏加德罗常数的值,则石墨晶体的层间距d=

a、b、c、d、e均为周期表前四周期元素,原子序数依次增大,相关信息如下表所示。
请回答:
(1)d属于________ 区的元素,其基态原子的价电子排布图为_________ 。
(2)b与其同周期相邻元素第一电离能由大到小的顺序为________ (用元素符号表示)。
(3)c的氢化物水溶液中存在的氢键有________ 种,任意画出一种________ 。
(4)a与其相邻同主族元素的最高价氧化物的熔点高低顺序为________ (用化学式表示)。若将a元素最高价氧化物水化物对应的正盐酸根离子表示为A,则A的空间构型为________ ;A的中心原子的轨道杂化类型为________ ;与A互为等电子体的一种分子为________ (填化学式)。
(5)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为________ ,若该晶体的相对分子质量为M,密度为ag/cm ,则晶胞的体积为
,则晶胞的体积为________ (NA用表示阿伏加 德罗常数的值)。
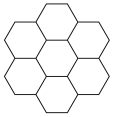
(6)a形成的某种单质的层状结构如图,其中a原子数、a—a键数、六元环数之比为____ 。
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 位于周期表中第4纵行 |
| e | 基态原子M层全充满,N层只有一个电子 |
请回答:
(1)d属于
(2)b与其同周期相邻元素第一电离能由大到小的顺序为
(3)c的氢化物水溶液中存在的氢键有
(4)a与其相邻同主族元素的最高价氧化物的熔点高低顺序为
(5)e与Au的合金可形成面心立方最密堆积的晶体,在晶胞中e原子处于面心,该晶体具有储氢功能,氢原子可进入到由e原子与Au原子构成的四面体空隙中,储氢后的晶胞结构与金刚石晶胞结构相似,该晶体储氢后的化学式为
 ,则晶胞的体积为
,则晶胞的体积为(6)a形成的某种单质的层状结构如图,其中a原子数、a—a键数、六元环数之比为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网