单选题 适中0.65 引用1 组卷59
某化学兴趣小组欲探究氢氧化镁固体在氯化铵中溶解的原因,进行了如下实验:
已知:① ;②常温下,
;②常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。
关于以上实验,下列说法错误的是
| 操作 | 实验序号 | 试剂X | 实验现象 |
| 实验一 | 白色浊液逐渐变澄清 | |
| 实验二 | 白色浊液变化不明显 | ||
| 实验三 | 白色浊液逐渐变澄清 | ||
| 实验四 | 白色浊液变化不明显 | ||
| 实验五 | 0.01mol/L蒸馏水,5.0mL | 白色浊液变化不明显 |
关于以上实验,下列说法错误的是
| A.只通过实验一和二,氢氧化镁溶解可能是铵根或者氢离子作用的结果 |
| B.若加入试剂X为0.1mol/LHCl溶液5mL,实验现象为白色浊液逐渐变澄清,与实验一形成对照,可以说明 |
| C.实验三和四中加入 |
| D.通过以上四个实验证明, |
2024·湖南·模拟预测
类题推荐
某小组拟设计实验探究金属氢氧化物在铵盐溶液中溶解度的影响因素。
已知:①常温下,几种氢氧化物的溶度积数据如下表所示:
②可能用到的试剂:
 溶液、
溶液、
 溶液、
溶液、
 溶液和
溶液和
 溶液;
溶液;
③常温下, 的电离常数
的电离常数 ,
, 的电离常数
的电离常数 。
。
实验一 比较 在不同浓度的
在不同浓度的 溶液中溶解情况。
溶液中溶解情况。
(1)实验结论是_______ 。
(2)针对实验(I),“白色浊液变澄清”的原因,提出如下假设:
假设①: ,
, ,
, 。
。
假设②: ,
,_______ (补充离子方程式)。
为了验证(2)提出的假设,设计如下实验:
实验二 比较 在不同浓度的
在不同浓度的 溶液中溶解情况。
溶液中溶解情况。
(3)选择 的理由是
的理由是_______ 。
实验结论是(2)中假设_______ 成立(填“①”或“②”)。
根据上述实验,有同学认为金属氢氧化物都能溶解于 溶液。为了验证他的观点,设计如下实验:
溶液。为了验证他的观点,设计如下实验:
实验三 探究 、、在
、、在 溶液中溶解情况。
溶液中溶解情况。
已知:(a) 、
、 、
、 都易溶于水,实验(Ⅵ)浊液变澄清可能的原因是
都易溶于水,实验(Ⅵ)浊液变澄清可能的原因是 更难电离;
更难电离;
(b)其他条件相同,难溶金属氢氧化物的溶解度越小,在同种铵盐溶液中溶解度越小。
(4)常温下, 、
、 、
、 溶解度由大到小排序为
溶解度由大到小排序为_______ 。
(5)通过上述实验,影响 在铵盐溶液中溶解度的因素主要有铵盐浓度、
在铵盐溶液中溶解度的因素主要有铵盐浓度、_______ 、_______ 。
已知:①常温下,几种氢氧化物的溶度积数据如下表所示:
③常温下,
实验一 比较
| 操作 | 试剂X | 现象 |
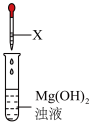 | (Ⅰ) | 白色浊液逐渐变澄清 |
| (Ⅱ) | 白色浊液变化不明显 |
(2)针对实验(I),“白色浊液变澄清”的原因,提出如下假设:
假设①:
假设②:
为了验证(2)提出的假设,设计如下实验:
实验二 比较
| 操作 | 试剂X | 现象 |
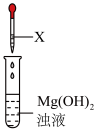 | (Ⅲ) | 白色浊液逐渐变澄清 |
| (Ⅳ) | 白色浊液变化不明显 |
实验结论是(2)中假设
根据上述实验,有同学认为金属氢氧化物都能溶解于
实验三 探究
| 操作 | Y | 现象 |
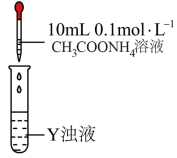 | (Ⅴ) | 没有明显现象 |
| (Ⅵ) | 浊液变澄清溶液 | |
| (Ⅶ) | 没有明显现象 |
(b)其他条件相同,难溶金属氢氧化物的溶解度越小,在同种铵盐溶液中溶解度越小。
(4)常温下,
(5)通过上述实验,影响
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网