解答题-工业流程题 适中0.65 引用3 组卷198
二氧化铈( )是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含
)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含 、
、 、
、 等)为原料制备
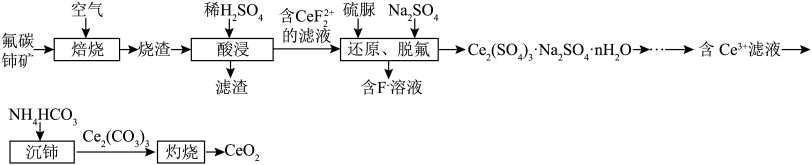
等)为原料制备 ,其工艺流程如图所示:
,其工艺流程如图所示:
(1)“焙烧”时,通入空气的主要目的是_________________ 。
(2)滤渣的主要成分是___________________ (填化学式)。
(3)“还原、脱氟”时,先加入硫脲(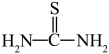 ),目的是将溶液中的
),目的是将溶液中的 还原为
还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_________________ [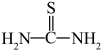 被氧化为
被氧化为 ,生成物还有HF和
,生成物还有HF和 ]。
]。
(4)“沉铈”时反应的离子方程式为__________________ 。若用 溶液代替
溶液代替 溶液,产生的后果是
溶液,产生的后果是________________ 。
(5)若常温下, ,
, ,
, 恰好沉淀完全
恰好沉淀完全 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中
_____________  。
。
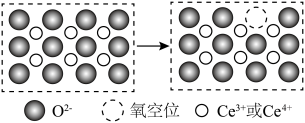
(6)二氧化铈作为一种SCR脱硝催化剂,能在 和
和 之间改变氧化状态,将
之间改变氧化状态,将 氧化为
氧化为 ,并引起氧空位的形成,得到新的铈氧化物
,并引起氧空位的形成,得到新的铈氧化物 。铈氧化物发生的可能变化如图所示。当
。铈氧化物发生的可能变化如图所示。当
 氧化标准状况下
氧化标准状况下 NO后,生成新的铈氧化物中x、y、z的最简整数比为
NO后,生成新的铈氧化物中x、y、z的最简整数比为____________ 。
(1)“焙烧”时,通入空气的主要目的是
(2)滤渣的主要成分是
(3)“还原、脱氟”时,先加入硫脲(
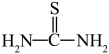 ),目的是将溶液中的
),目的是将溶液中的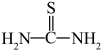 被氧化为
被氧化为(4)“沉铈”时反应的离子方程式为
(5)若常温下,
(6)二氧化铈作为一种SCR脱硝催化剂,能在
2024·河南信阳·模拟预测
类题推荐
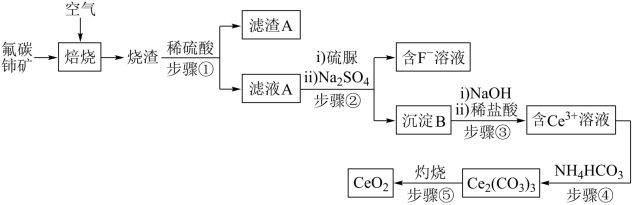
氧化铈(CeO2)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:

已知:
①Ce4+能与 结合成
结合成 ,也能与
,也能与 结合成
结合成 ;
;
②Ce3+和Na2SO4形成复盐沉淀,Ce3+在空气中易被氧化为Ce4+;
③硫脲(SCN2H4)具有还原性,酸性条件下易被氧化为(SCN2H3)2。
回答下列问题:
(1)焙烧后,Ce元素转化成CeO2和CeF4,写出焙烧的化学方程式:_______ 。
(2)滤渣A的主要成分是_______ 。
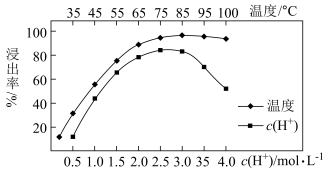
(3)步骤①加入稀硫酸浸出,Ce的浸出率与c(H+)、温度的关系如图所示,应选择的适宜的条件为_______(填标号)。
(4)写出步骤②中第(i)步加入硫脲还原[CeSO4]2+的离子方程式为_______ 。
(5)CeFCO3在氧化焙烧时会产生一种气体,该气体溶于水后能腐蚀玻璃的原因是_______ (用化学方程式表示)。
(6)常温下,若步骤④中Ce3+恰好沉淀完全[ 为
为 ,此时测得溶液的pH=5,则溶液中
,此时测得溶液的pH=5,则溶液中
_______  {已知常温下
{已知常温下 ,
, 。
。

已知:
①Ce4+能与
②Ce3+和Na2SO4形成复盐沉淀,Ce3+在空气中易被氧化为Ce4+;
③硫脲(SCN2H4)具有还原性,酸性条件下易被氧化为(SCN2H3)2。
回答下列问题:
(1)焙烧后,Ce元素转化成CeO2和CeF4,写出焙烧的化学方程式:
(2)滤渣A的主要成分是
(3)步骤①加入稀硫酸浸出,Ce的浸出率与c(H+)、温度的关系如图所示,应选择的适宜的条件为_______(填标号)。

| A. | B. | C. | D. |
(5)CeFCO3在氧化焙烧时会产生一种气体,该气体溶于水后能腐蚀玻璃的原因是
(6)常温下,若步骤④中Ce3+恰好沉淀完全[
氧化铈(CeO2)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:
已知:①Ce4+能与F-结合成[CeFx](4-x)+,也能与SO 结合成[CeSO4]2+;
结合成[CeSO4]2+;
②Ce3+和Na2SO4形成复盐沉淀,Ce3+在空气中易被氧化为Ce4+;
③硫脲(SCN2H4)具有还原性,酸性条件下易被氧化为(SCN2H3)2。
回答下列问题:
(1)焙烧后,Ce元素转化成CeO2和CeF4,写出焙烧的化学方程式___________ 。
(2)滤渣A的主要成分是___________ 。
(3)步骤①加入稀硫酸浸出,Ce的浸出率与c(H+)、温度的关系如图所示,应选择的适宜的条件为___________(填序号)。

(4)写出步骤②中加入硫脲还原[CeSO4]2+的离子方程式为___________ 。
(5)步骤③加入盐酸后,通常还需加入H2O2,其主要目的为___________ 。
(6)步骤④中若Ce3+恰好沉淀完全(c(Ce3+)为1.0×10-5mol·L-1),此时测得溶液的,pH=5,则溶液中c(HCO )=
)=___________ mol·L-1(保留3位小数)。(已知常温下ka2(H2CO3)=5.61×10-11,Ksp[Ce2(CO3)3]=1.0×10-28)

已知:①Ce4+能与F-结合成[CeFx](4-x)+,也能与SO
②Ce3+和Na2SO4形成复盐沉淀,Ce3+在空气中易被氧化为Ce4+;
③硫脲(SCN2H4)具有还原性,酸性条件下易被氧化为(SCN2H3)2。
回答下列问题:
(1)焙烧后,Ce元素转化成CeO2和CeF4,写出焙烧的化学方程式
(2)滤渣A的主要成分是
(3)步骤①加入稀硫酸浸出,Ce的浸出率与c(H+)、温度的关系如图所示,应选择的适宜的条件为___________(填序号)。

| A.65℃ 2.0mol·L-1 | B.75℃ 2.0mol·L-1 |
| C.85℃ 2.5mol·L-1 | D.100℃ 2.5mol·L-1 |
(5)步骤③加入盐酸后,通常还需加入H2O2,其主要目的为
(6)步骤④中若Ce3+恰好沉淀完全(c(Ce3+)为1.0×10-5mol·L-1),此时测得溶液的,pH=5,则溶液中c(HCO
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网





