单选题 适中0.65 引用1 组卷100
除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有 和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受H2O的H+进攻。其中SiCl4的亲核水解机理如图。下列说法错误的是
和有空的价轨道;发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受H2O的H+进攻。其中SiCl4的亲核水解机理如图。下列说法错误的是
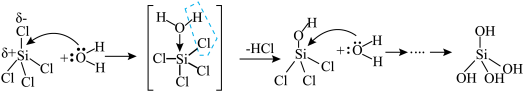
| A.上述过程Si的杂化方式发生了改变 | B.根据上述机理,NF3不能发生水解 |
| C.预测NCl3能发生亲电水解 | D.CCl4的水解机理与上述过程类似 |
2024·安徽安庆·三模
类题推荐
非金属的卤化物水解可以分为亲电水解和亲核水解,实例及部分机理示意如下:发生亲电水解的条件是中心原子具有孤电子对,能接受H2O的H+的进攻,如: 和空的价层轨道,接受H2O的孤电子对进攻,如:
和空的价层轨道,接受H2O的孤电子对进攻,如:


| A.NCl3和SiCl4水解过程中中心原子的杂化方式不变 |
| B.推测CCl4比SiCl4难发生亲核水解 |
| C.推测NF3比NCl3难发生亲电水解: |
| D.已知AsCl3的水解产物为H3AsO3和HCl,推测其水解类型为亲核水解 |
共价化合物的水解分为亲电水解和亲核水解。发生亲电水解的条件是中心原子具有孤电子对,能接受H2O的H+的进攻,例如:


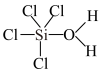
 _____→
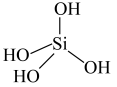
_____→
| A.NF3分子中F原子电负性大,N原子难以给出孤电子对,所以较难发生亲电水解 |
| B.CCl4分子中C原子外围空间小,且没有能量较低的空轨道,所以较难发生亲核水解 |
| C.预测SF4的水解产物为SO2和HF |
| D.已知AsCl3的水解产物为H3AsO3和HC1,所以水解类型为亲电水解 |
SiCl4可发生水解反应,机理如下所示。下列说法错误的是
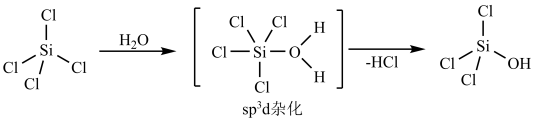

| A.CCl4与SiCl4均是正四面体结构,稳定性SiCl4大于CCl4 |
| B.CCl4与SiCl4均属于分子晶体,CCl4不能按照上述机理发生水解反应 |
| C.SiCl4与H2O的中心原子均采取sp3杂化,键角:SiCl4大于H2O |
| D.基态Si原子核外有8种能量不同的电子 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


