解答题-工业流程题 适中0.65 引用1 组卷40
以湿法炼锌厂所产的钴锰渣(主要成分为 、
、 、
、 、
、 ,含少量
,含少量 、
、 、
、 、
、 等)为原料回收制备
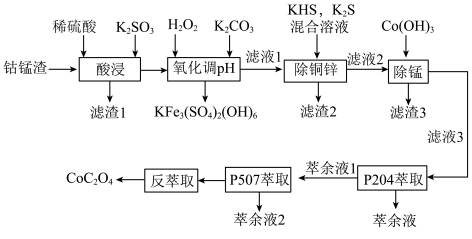
等)为原料回收制备 的工艺如下:
的工艺如下: ,
, ,
, 。
。
回答下列问题:
(1)“酸浸”时可能产生有毒气体_______ ,说出该气体的一种用途_______ 。
(2)“氧化调pH”过程中得到 沉淀的离子方程式为
沉淀的离子方程式为_______ 。
(3)若 溶液的
溶液的 ,试分析
,试分析 主要以
主要以______ [填“ ”或“
”或“ ”]形式除去,通过计算说明你的理由
”]形式除去,通过计算说明你的理由______ 。
(4)“滤渣3”中含有S、 ,写出得到
,写出得到 的化学方程式
的化学方程式______ 。
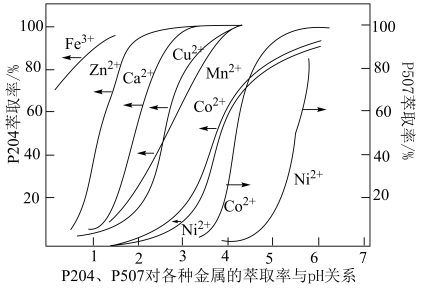
(5)P5O4、P5O7对金属离子的萃取率与pH的关系如图所示。______ 。
②“萃余液2”中的主要成分为______ (填化学式),指出分离钴镍的合适pH范围为______ (填标号)。
A.3~4 B.4~5 C.5~6 D.6~7
回答下列问题:
(1)“酸浸”时可能产生有毒气体
(2)“氧化调pH”过程中得到
(3)若
(4)“滤渣3”中含有S、
(5)P5O4、P5O7对金属离子的萃取率与pH的关系如图所示。
②“萃余液2”中的主要成分为
A.3~4 B.4~5 C.5~6 D.6~7
2024·山西太原·一模
类题推荐
钴被誉为战略物资,有出色的性能和广泛的应用.以水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、A12O3、MnO等)制取钴产品的工艺流程如下:

已知:
①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、A13+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
回答下列问题:
(1)写出浸出过程、Co2O3发生反应的离子方程式:_________________________ 。
(2)写出NaClO3发生反应的主要离子方程式:______________________________ ;
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为____________________________ 。
(4)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是_________________ ;萃取剂使用的最佳pH范围是__________ (填代号)。
A.1.0~1.5 B.2.0~2.5 C.3.0~3.5 D.4.0~4.5

(5)“沉钴”时生成CoCO3的离子方程式为__________________________________ 。
(6)在空气中焙烧CoCO3生成CoxOy和CO2,测得充分煅烧后固体质量为4.82g,CO2的体积为1.344L(标准状况),则CoxOy的化学式为___________________ 。

已知:
①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、A13+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Mn(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
回答下列问题:
(1)写出浸出过程、Co2O3发生反应的离子方程式:
(2)写出NaClO3发生反应的主要离子方程式:
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为
(4)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是
A.1.0~1.5 B.2.0~2.5 C.3.0~3.5 D.4.0~4.5

(5)“沉钴”时生成CoCO3的离子方程式为
(6)在空气中焙烧CoCO3生成CoxOy和CO2,测得充分煅烧后固体质量为4.82g,CO2的体积为1.344L(标准状况),则CoxOy的化学式为
CoCl2常作湿度指示剂、分析试剂等。以钴渣(主要成分是CoO、Co2O3,含少量Ni、SiO2、Al2O3等杂质)为原料制备无水氯化钴(CoCl2)的流程如图(部分产物和条件省略):
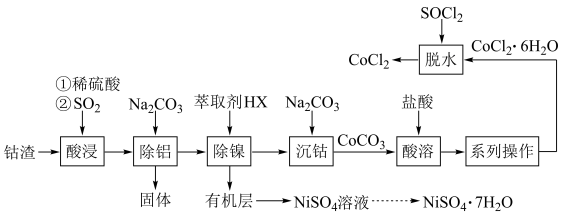
已知:① 几种金属离子转化为氢氧化物沉淀的pH如表所示:
② SOCl2易水解生成两种气体,其中一种气体能使品红溶液褪色。
回答下列问题:
(1)“酸浸”中提高反应速率的措施是_________________________ (答一点即可);SO2的作用是________________ ,其发生反应的离子方程式为________________ 。
(2)“除铝”得到固体的主要成分是______ (填化学式),该步调节pH的范围为_______ 。
(3)“除镍”中分离有机层的操作若在实验室中进行,需要使用的玻璃仪器为______ (填名称)。
(4)“系列操作”包括__________ 、_________ 、过滤、洗涤等。
(5)在加热条件下“脱水”,写出该过程中总反应的化学方程式:____________________ 。

已知:① 几种金属离子转化为氢氧化物沉淀的pH如表所示:
金属离子 | Al3+ | Co2+ | Ni2+ |
开始沉淀的pH | 4.0 | 7.6 | 7.7 |
完全沉淀的pH | 5.2 | 9.2 | 9.5 |
回答下列问题:
(1)“酸浸”中提高反应速率的措施是
(2)“除铝”得到固体的主要成分是
(3)“除镍”中分离有机层的操作若在实验室中进行,需要使用的玻璃仪器为
(4)“系列操作”包括
(5)在加热条件下“脱水”,写出该过程中总反应的化学方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



