解答题-工业流程题 较难0.4 引用1 组卷65
一种从分银渣(含CuO、 、
、 、
、 、
、 、Ag、
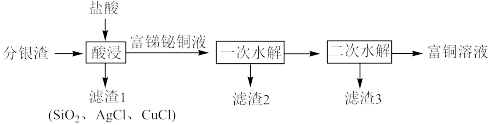
、Ag、 等)回收金属资源的工艺流程如下:
等)回收金属资源的工艺流程如下:
Ⅰ.CuCl难溶于水,但溶于浓盐酸。
Ⅱ.“富锑铋铜液”中含 (铋离子)、
(铋离子)、 (锑离子)、
(锑离子)、 、
、 。
。
Ⅲ.该工艺条件下,有关金属离子沉淀时的相关pH见下表:
回答下列问题:
(1)写出分银渣中的Ag与盐酸、溶解氧反应的离子方程式:___________________ 。
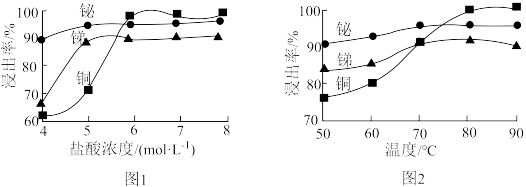
(2)“酸浸”时,盐酸浓度对锑、铋、铜浸出率的影响如图1所示,温度对锑、铋、铜浸出率的影响如图2所示。______ ;浸出时温度以80℃为宜,其原因是_____________________ 。
(3)①已知“滤渣2”的主要成分是 ,则“一次水解”时主要发生反应的化学方程式为
,则“一次水解”时主要发生反应的化学方程式为________ 。
②已知“滤渣3”的主要成分是BiOCl和 ,则“二次水解”时调节pH的范围应该是
,则“二次水解”时调节pH的范围应该是______ 。
(4)“滤渣1”中的AgCl可用硫酸-硫脲(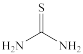 )浸出,生成配合物
)浸出,生成配合物 ,写出该反应的化学方程式:
,写出该反应的化学方程式:________________ ;该配合物中不存在__________ (填标号)。
A.离子键 B.极性共价键 C.配位键 D.范德华力 E.非极性共价键
(5)写出一种从“富铜溶液”中回收金属资源的方法:_________________ 。
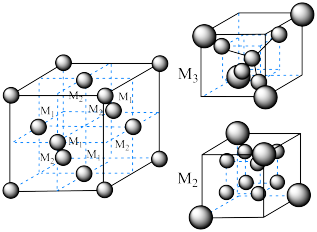
(6)尖晶石属于立方晶系,其晶胞可视为 、
、 两种结构交替无隙并置而成(如图所示),其中
两种结构交替无隙并置而成(如图所示),其中 可以为
可以为 、
、 、
、 、
、 等,
等, 可以为
可以为 、
、 、
、 等。已知尖晶石型
等。已知尖晶石型 的晶胞参数为842pm,则该晶体的密度为
的晶胞参数为842pm,则该晶体的密度为________  。(列出计算式,阿伏加德罗常数的值为
。(列出计算式,阿伏加德罗常数的值为 )
)
Ⅰ.CuCl难溶于水,但溶于浓盐酸。
Ⅱ.“富锑铋铜液”中含
Ⅲ.该工艺条件下,有关金属离子沉淀时的相关pH见下表:
金属离子 | ||||
开始沉淀时( | 0.5 | 1.5 | 4.7 | 1.5 |
完全沉淀时( | 1.4 | 2.5 | 6.7 | 3.2 |
(1)写出分银渣中的Ag与盐酸、溶解氧反应的离子方程式:
(2)“酸浸”时,盐酸浓度对锑、铋、铜浸出率的影响如图1所示,温度对锑、铋、铜浸出率的影响如图2所示。
(3)①已知“滤渣2”的主要成分是
②已知“滤渣3”的主要成分是BiOCl和
(4)“滤渣1”中的AgCl可用硫酸-硫脲(
 )浸出,生成配合物
)浸出,生成配合物A.离子键 B.极性共价键 C.配位键 D.范德华力 E.非极性共价键
(5)写出一种从“富铜溶液”中回收金属资源的方法:
(6)尖晶石属于立方晶系,其晶胞可视为
2024·山西太原·三模
类题推荐
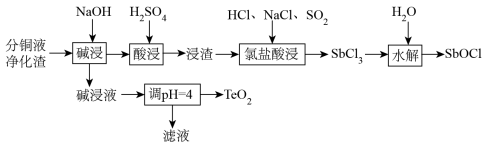
分铜液净化渣主要含铜、碲(Te)、锑(Sb)、砷(As)等元素的化合物,一种回收工艺流程如图所示。

已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
③查阅资料得知:离子晶体的熔点一般较高,在600~2000℃,共价晶体具有较高的熔点,一般在1000℃以上。
回答下列问题:
(1)基态As的价层电子轨道表示式为_______ 。
(2)“碱浸”时,TeO2与NaOH反应的离子方程式为______ 。
(3)向碱浸液中加盐酸调节pH=4,有TeO2析出,分离TeO2,滤液中As元素最主要的存在形式为_______ (常温下,H3AsO4的各级电离常数:Ka1=6.3×10-3、Ka2=1.0×10-7、Ka3=3.2×10-12,填字母)。
(4)“氯盐酸浸”时,通入SO2的目的是_______ 。
(5)“水解”时,生成SbOCl的化学方程式为_______ 。
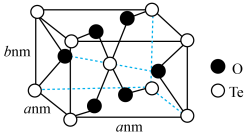
(6)TeO2可用作电子元件材料,熔点为733℃,其熔点远高于SO2的原因为______ 。TeO2晶胞是长方体结构(如图所示),已知NA为阿伏加德罗常数的值,则该晶体的密度为______ g•cm-3(列出计算表达式)。


已知:①“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有Na2TeO3、Na3AsO4。
②“酸浸”时,锑元素反应生成难溶的Sb2O(SO4)4浸渣。
③查阅资料得知:离子晶体的熔点一般较高,在600~2000℃,共价晶体具有较高的熔点,一般在1000℃以上。
回答下列问题:
(1)基态As的价层电子轨道表示式为
(2)“碱浸”时,TeO2与NaOH反应的离子方程式为
(3)向碱浸液中加盐酸调节pH=4,有TeO2析出,分离TeO2,滤液中As元素最主要的存在形式为
| A.H3AsO4 | B.H2As | C.HAsO | D.AsO |
(4)“氯盐酸浸”时,通入SO2的目的是
(5)“水解”时,生成SbOCl的化学方程式为
(6)TeO2可用作电子元件材料,熔点为733℃,其熔点远高于SO2的原因为

电解锰渣的主要成分为MnS、 、
、 ,还含有少量
,还含有少量 、CaO、
、CaO、 、
、 等氧化物。一种回收电解锰渣制备高纯度
等氧化物。一种回收电解锰渣制备高纯度 晶体的部分工艺流程如下:
晶体的部分工艺流程如下:

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
(1)为了提高锰的浸出率,“酸浸氧化”时可采取的措施为______ (写出一种即可)。
(2)滤渣①的成分是______ 。
(3)“酸浸氧化”时电解锰渣中的MnS转化为 ,该反应的化学方程式为
,该反应的化学方程式为______ 。
(4)萃取剂①对金属离子的萃取率与pH的关系如图所示,萃取剂①使用的适宜pH范围是______ (填字母)。萃取原理为 (油相)
(油相) (油相)
(油相) ,向油相②加入硫酸能进行反萃取的原因是
,向油相②加入硫酸能进行反萃取的原因是______ (用平衡移动原理解释)。

A. 0.5~1.0 B. 1.5~2.5
C. 3.0~4.0 D. >4.0
(5)pH=5时,溶液中残余的 的浓度为
的浓度为______  (列出计算式即可)。
(列出计算式即可)。
(6)电解酸性硫酸锰可制备二氧化锰,阳极的电极反应式为______ 。
(7)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为______ 。该晶体的密度为 ,则晶体中相邻N之间的最短距离为
,则晶体中相邻N之间的最短距离为______ nm(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。


溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | |||
开始沉淀时( | 2.2 | 3.7 | 8.6 |
沉淀完全时( | 3.2 | 4.7 | 10.1 |
(2)滤渣①的成分是
(3)“酸浸氧化”时电解锰渣中的MnS转化为
(4)萃取剂①对金属离子的萃取率与pH的关系如图所示,萃取剂①使用的适宜pH范围是

A. 0.5~1.0 B. 1.5~2.5
C. 3.0~4.0 D. >4.0
(5)pH=5时,溶液中残余的
(6)电解酸性硫酸锰可制备二氧化锰,阳极的电极反应式为
(7)某种含锰特殊材料的晶胞结构如图所示,该晶体的化学式为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网