解答题-原理综合题 适中0.65 引用1 组卷521
A.O2和O3 B.12C和13C C.CH3CH2CH2CH3和CH3CH(CH3)2
D.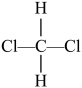 和
和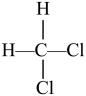 E.CH3CH2CH2CH3和CH3CH2CH(CH3)2
E.CH3CH2CH2CH3和CH3CH2CH(CH3)2
(1)
(2)从能量变化角度研究反应
A. 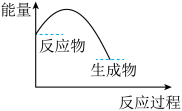 B.
B.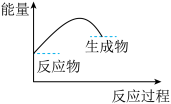
| 化学键 | H—H | O=O | H—O |
| 键能(kJ/mol) | 436 | 496 | 463 |
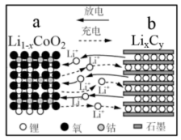
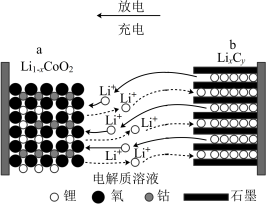
(4)传统汽车中使用的电池主要是铅酸蓄电池,其构造如图所示,该电池的工作原理为
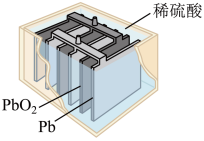
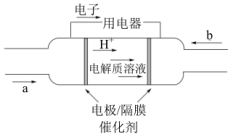
(5)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:
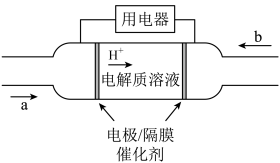
②电池每消耗标准状况下5.6L氢气,电路中通过的电子数目为
23-24高一下·天津·期中
类题推荐
化学反应是人类获取能量的重要途径,我们可以通过化学反应实现化学能向热能、电能的直接转化。
I.回答下列问题:
(1)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
则常温常压下,1mol H2 在空气中充分燃烧,生成 1mol H2O (g)放出热量______ kJ。
II.各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
(2)传统汽车中使用的电池主要是铅蓄电池,其构造如图所示。
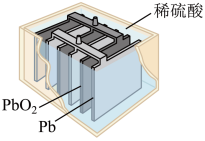
①电池工作时,电子由___________ 流出(填“Pb”或“ PbO2”)
②该电池的工作原理为 ,其工作时电解质溶液的 pH 将
,其工作时电解质溶液的 pH 将___________ (填“增大”“减小”或“不变”)。
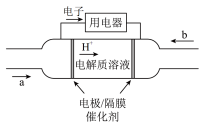
(3)2020 年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:
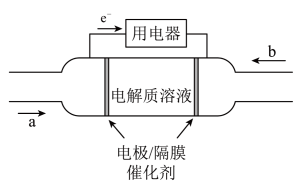
①a 处通入的气体是___________ ;
②电池每消耗标准状况下 5.6L 氢气,电路中通过的电子数目为___________ 。
III.为了更好地利用化学反应中物质和能量的变化,在化学研究和工业生产中还需要关注化学反应的快慢和限度。能量、速率与限度是认识和研究化学反应的重要因素。某温度下,向2.0L 的恒容密闭容器中充入 2.0mol N2 和 2.0mol H2 ,发生反应,实验数据如下表所示:
(4)0~50s 内的平均反应速率v(N2)=___________ 。
(5)为加快反应速率,可采取的措施是___________ (填字母)。
a.升高温度 b.增大容器体积 c.加入合适的催化剂
I.回答下列问题:
(1)从断键和成键角度分析上述反应中能量的变化。部分化学键的键能如下表:
| 化学键 | H-H | 0=0 | H-O |
| 键能(kJ/mol) | 436 | 496 | 463 |
II.各类电池广泛用在交通工具(如电动汽车、电动自行车等)上,实现了节能减排,也为生活带来了极大的便利。
(2)传统汽车中使用的电池主要是铅蓄电池,其构造如图所示。

①电池工作时,电子由
②该电池的工作原理为
(3)2020 年上海进博会展览中,诸多氢能源汽车纷纷亮相,氢氧燃料电池被誉为氢能源汽车的心脏。某种氢氧燃料电池的内部结构如图所示:

①a 处通入的气体是
②电池每消耗标准状况下 5.6L 氢气,电路中通过的电子数目为
III.为了更好地利用化学反应中物质和能量的变化,在化学研究和工业生产中还需要关注化学反应的快慢和限度。能量、速率与限度是认识和研究化学反应的重要因素。某温度下,向2.0L 的恒容密闭容器中充入 2.0mol N2 和 2.0mol H2 ,发生反应,实验数据如下表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(4)0~50s 内的平均反应速率v(N2)=
(5)为加快反应速率,可采取的措施是
a.升高温度 b.增大容器体积 c.加入合适的催化剂
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网