解答题-原理综合题 困难0.15 引用1 组卷128
乙醛 是一种常见的有机物,在生产、生活中用途广泛。回答下列问题:
是一种常见的有机物,在生产、生活中用途广泛。回答下列问题:
(1)已知:①
②
③

_______ 。
(2)在镍催化下,乙醛与氢气反应生成乙醇。在恒温恒容反应器中充入一定量 和
和 发生反应:
发生反应: 。下列叙述错误的是_______(填标号)。
。下列叙述错误的是_______(填标号)。
(3) 速率方程
速率方程 (k为速率常数,只与温度、催化剂有关;n为反应级数)。
(k为速率常数,只与温度、催化剂有关;n为反应级数)。
①阿伦尼乌斯就关于速率常数与活化能 、温度(T)的关系提出经验关系式:
、温度(T)的关系提出经验关系式: (R为常数,k为速率常数,
(R为常数,k为速率常数, 为活化能,T为温度)。一定温度下,在
为活化能,T为温度)。一定温度下,在 (催化剂)作用下,
(催化剂)作用下, 与
与 关系如图所示。
关系如图所示。_______ (填“ ”或“
”或“ ”),判断依据是
”),判断依据是_______ 。
②为了测定反应级数(n),实验测得 在一系列不同浓度时的初始反应速率数据如下:
在一系列不同浓度时的初始反应速率数据如下:
已知:一步进行的反应称为基元反应,基元反应中反应级数等于反应物的化学计量数之和。下列叙述正确的是_______ (填标号)。
A.该总反应为二级反应
B.速率常数
C.上述反应不是基元反应
D. 时
时
(4)一定温度下,保持总压强为 ,向反应器充入
,向反应器充入 和
和 的混合气体(
的混合气体( 不参与反应)发生反应
不参与反应)发生反应 ,测得
,测得 平衡转化率与起始投料比
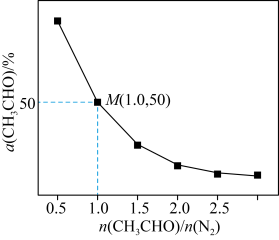
平衡转化率与起始投料比 的关系如图所示。
的关系如图所示。 的平衡转化率随着投料比增大而减小的原因是
的平衡转化率随着投料比增大而减小的原因是_______ 。该温度下,上述反应M点平衡常数
_______  。(
。( 为用分压计算的平衡常数,分压=总压×物质的量分数)
为用分压计算的平衡常数,分压=总压×物质的量分数)
(5) 时,向反应器充入一定量
时,向反应器充入一定量 发生反应
发生反应 ,测得单位时间内
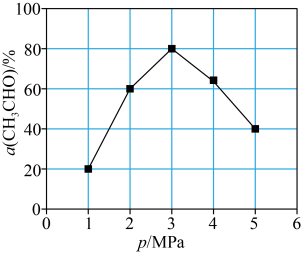
,测得单位时间内 转化率与压强关系如图所示。解释
转化率与压强关系如图所示。解释 时
时 的转化率达到峰值的原因:
的转化率达到峰值的原因:_______ 。 制备乙醛,其阴极的电极反应式为
制备乙醛,其阴极的电极反应式为_______ 。
(1)已知:①
②
③
(2)在镍催化下,乙醛与氢气反应生成乙醇。在恒温恒容反应器中充入一定量
| A.气体压强不随时间变化时达到平衡状态 |
| B.平衡后充入氖气,平衡向逆反应方向移动 |
| C.上述可逆反应的正反应是嫡增反应 |
| D.平衡后,充入少量 |
(3)
①阿伦尼乌斯就关于速率常数与活化能

②为了测定反应级数(n),实验测得
| 0.1 | 0.2 | 0.3 | 0.4 | |
| 0.020 | 0.080 | 0.182 | 0.318 |
A.该总反应为二级反应
B.速率常数
C.上述反应不是基元反应
D.
(4)一定温度下,保持总压强为
(5)
2024·河南·模拟预测
类题推荐
乙醇是一种绿色能源,也是一种化工原料。
(1)已知几种热化学方程式如下:
①

②

③

(ⅰ)上述反应中,在任意温度下都能自发进行的是___________ (填序号)。
(ⅱ)我国科学家开发新型催化剂利用乙醇直接制备乙酸乙酯:

___________  。
。
(2)乙醇是一种储氢材料。
 ,Akande对其动力学机理的研究(*代表物种吸附在催化剂表面上)如图所示:
,Akande对其动力学机理的研究(*代表物种吸附在催化剂表面上)如图所示:
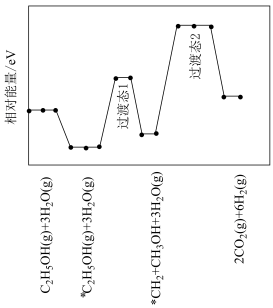
①
___________ 0(填“>”“<”或“=”),总反应分___________ 步反应进行。
②速控反应的方程式为___________ 。
(3)一定温度下,向恒容密闭容器中充入适量乙醇蒸气,发生反应: ,下列叙述正确的是___________(填标号)。
,下列叙述正确的是___________(填标号)。
(4)保持总压为 ,向反应器中充入乙醇
,向反应器中充入乙醇 和氮气(不参与反应),发生反应:
和氮气(不参与反应),发生反应: ,测得乙醇的平衡转化率与投料比
,测得乙醇的平衡转化率与投料比 、温度
、温度 的关系如图所示:
的关系如图所示:
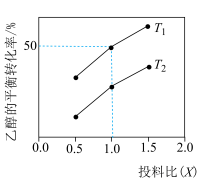
①其他条件不变时,随着 增大,乙醇的平衡转化率增大的原因是
增大,乙醇的平衡转化率增大的原因是_______ ,
_____  (填“>”或“<”)。
(填“>”或“<”)。
② 温度下,投料比为1.0时,平衡常数
温度下,投料比为1.0时,平衡常数 为
为________  (提示:用分压计算的平衡常数为
(提示:用分压计算的平衡常数为 ,分压
,分压 总压
总压 物质的显分数)。
物质的显分数)。
(5)我国科学家开发复合催化剂,实现了在酸性条件下电还原 制备乙醇,阴极反应式为
制备乙醇,阴极反应式为___________ 。
(1)已知几种热化学方程式如下:
①
②
③
(ⅰ)上述反应中,在任意温度下都能自发进行的是
(ⅱ)我国科学家开发新型催化剂利用乙醇直接制备乙酸乙酯:
(2)乙醇是一种储氢材料。

①
②速控反应的方程式为
(3)一定温度下,向恒容密闭容器中充入适量乙醇蒸气,发生反应:
| A.当气体总压强不变时,达到平衡状态 |
| B.平衡时升温,正反应速率大于逆反应速率 |
| C.平衡时,充入氩气,平衡向左移动 |
| D.平衡时,充入少量 |
(4)保持总压为

①其他条件不变时,随着
②
(5)我国科学家开发复合催化剂,实现了在酸性条件下电还原
科学家开发催化剂实现 催化还原制备附加值高的产品。利用
催化还原制备附加值高的产品。利用 制备甲醇的有关反应如下:
制备甲醇的有关反应如下:
Ⅰ.
Ⅱ.
(1)已知几种共价键的键能如下:
利用键能数据计算:
___________  。
。
(2)一定温度下,在恒容密闭容器中充入等体积的 、
、 ,仅发生反应Ⅰ,下列叙述正确的是
,仅发生反应Ⅰ,下列叙述正确的是___________ (填标号)。
A.平衡后充入氦气,正反应速率增大
B. 的体积分数不变时达到平衡状态
的体积分数不变时达到平衡状态
C.平衡后充入少量 ,
, 平衡转化率增大
平衡转化率增大
(3)在一恒容反应器中充入一定量的 、
、 ,仅发生反应Ⅱ,平衡常数(K)与温度(T)的关系如下:
,仅发生反应Ⅱ,平衡常数(K)与温度(T)的关系如下:
①
___________ (填“>”“<”或“=”)0。
②1200℃时,某时刻反应体系中 ,
, ,此时平衡
,此时平衡___________ (填“向正反应方向”“向逆反应方向”或“不”)移动。
(4)一定条件下,速率常数与活化能、温度的关系式为 +C(R、C为常数,
+C(R、C为常数, 为速率常数,
为速率常数, 为活化能,T为温度)。一定温度下,合成甲醇的速率常数在不同催化剂(Catl、Cat2)作用下,与温度的关系如图1所示。
为活化能,T为温度)。一定温度下,合成甲醇的速率常数在不同催化剂(Catl、Cat2)作用下,与温度的关系如图1所示。 为
为___________  ;催化效果更好的是
;催化效果更好的是___________ (填“Cat1”或“Cat2”)。
(5)在一定温度下,向甲、乙两密闭反应器中分别充入 和
和 ,分别在有水分子隔离膜、无水分子隔离膜作用下发生上述两个反应,测得
,分别在有水分子隔离膜、无水分子隔离膜作用下发生上述两个反应,测得 平衡转化率与压强的关系如图2所示。
平衡转化率与压强的关系如图2所示。___________ (填“甲”或“乙”),理由是___________ 。
②已知M点 选择性为80%,该温度下,M点反应Ⅱ的平衡常数
选择性为80%,该温度下,M点反应Ⅱ的平衡常数 为
为___________ (结果保留三位有效数字)。提示:分压=总压×物质的量分数, 选择性等于
选择性等于 的物质的量与
的物质的量与 转化的总物质的量之比。
转化的总物质的量之比。
Ⅰ.
Ⅱ.
(1)已知几种共价键的键能如下:
| 共价键 | |||||
| 键能/(kJ/mol) | 799 | 436 | 413 | 358 | 467 |
(2)一定温度下,在恒容密闭容器中充入等体积的
A.平衡后充入氦气,正反应速率增大
B.
C.平衡后充入少量
(3)在一恒容反应器中充入一定量的
| 700 | 800 | 830 | 1000 | 1200 | |
| 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②1200℃时,某时刻反应体系中
(4)一定条件下,速率常数与活化能、温度的关系式为

(5)在一定温度下,向甲、乙两密闭反应器中分别充入

②已知M点
在催化剂作用下, 发生如下反应:
发生如下反应:
①

②

回答下列问题:
(1)

___________  。
。
(2)一定温度下,向恒容密闭容器中充入 和
和 发生反应①,达到平衡时
发生反应①,达到平衡时 转化率为20%。下列叙述正确的是___________(填标号)。
转化率为20%。下列叙述正确的是___________(填标号)。
(3) 和
和 在催化剂作用下能发生反应:
在催化剂作用下能发生反应:
 。在1L恒容密闭容器中充入
。在1L恒容密闭容器中充入 和
和 ,测定
,测定 平衡转化率、催化效率与温度的关系如图1所示。
平衡转化率、催化效率与温度的关系如图1所示。
___________ (填“>”“<”或“=”)0。
②温度高于400℃,催化效率降低的原因是___________ 。T点平衡常数K___________ (填“>”“<”或“=”)0.5。
(4)在恒温条件下,向反应器充入 和
和 发生反应①,测得平衡时
发生反应①,测得平衡时 和
和 的物质的量浓度与平衡总压强的关系如图2所示。表示平衡时
的物质的量浓度与平衡总压强的关系如图2所示。表示平衡时 的物质的量浓度与平衡总压强的关系的是曲线
的物质的量浓度与平衡总压强的关系的是曲线___________ (填“ ”或“
”或“ ”)。M点时该反应的压强平衡常数
”)。M点时该反应的压强平衡常数
___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。 制备乙炔,其阴极的电极反应式为
制备乙炔,其阴极的电极反应式为___________ 。
①
②
回答下列问题:
(1)
(2)一定温度下,向恒容密闭容器中充入
| A.当 |
| B.上述反应达到平衡时放出热量为131.2kJ |
| C.平衡时向容器充入氩气,逆反应速率大于正反应速率 |
| D.加入催化剂,正反应速率等于逆反应速率且都增大 |
(3)

②温度高于400℃,催化效率降低的原因是
(4)在恒温条件下,向反应器充入

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


