解答题-工业流程题 较难0.4 引用2 组卷167

| 物质 | ||||
| 物质 | ||||
(1)“酸浸”中提高反应速率的可行措施有
(2)加入
(3)回收的沉淀可与浓硫酸反应生成能腐蚀玻璃的气体,
(4)用去离子水多次洗涤
(5)“高压釜水热反应”溶液pH应调节为中性,而不能过高的原因是
2024·重庆·模拟预测
类题推荐  是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有少量
,还含有少量 、FeO、CoO、
、FeO、CoO、 )为原料制备
)为原料制备 的工艺流程如图。
的工艺流程如图。
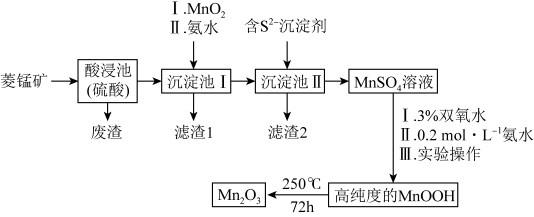
已知:25℃时,相关物质的 见表。
见表。
已知:氢氧化氧锰(MnOOH)难溶于水和碱性溶液。
(1)MnOOH中Mn的化合价为___________ 价。加快酸浸速率的措施___________ 。
(2)向“沉淀池Ⅰ”中加入 ,
, 的作用是
的作用是___________ (用离子方程式回答);“滤渣2”的主要成分是___________ (填化学式)。
(3) 转化为MnOOH的离子方程式为
转化为MnOOH的离子方程式为___________ 。
(4) 转化为MnOOH中“Ⅲ。实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
转化为MnOOH中“Ⅲ。实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为___________ 。
(5)高纯度的MnOOH转化为 的化学方程式为
的化学方程式为___________ 。
(6)在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为___________ (当溶液中某离子浓度 mol⋅L
mol⋅L 时。可认为该离子沉淀完全)。
时。可认为该离子沉淀完全)。

已知:25℃时,相关物质的
| 物质 | |||||
(1)MnOOH中Mn的化合价为
(2)向“沉淀池Ⅰ”中加入
(3)
(4)
(5)高纯度的MnOOH转化为
(6)在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀,则理论上pH的最小值为
Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量Fe3O4、FeO、CoO、Al2O3)为原料制备Mn2O3的工艺流程如图。已知:
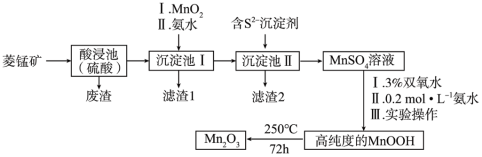
①25℃时相关物质的Ksp见下表。
②氢氧化氧锰(MnOOH)难溶于水和碱性溶液;“沉淀池Ⅰ”的条件下,Co2+不能被二氧化锰氧化。
(1)为提高“酸浸”的效率,可以采取的措施为_______ 。(写一种)
(2)向“沉淀池Ⅰ”中加入MnO2,MnO2的作用是_______ ;“滤渣2”的主要成分是_______ (填化学式)。
(3)MnSO4转化为MnOOH的离子方程式为_______ 。
(4)MnSO4转化为MnOOH中“Ⅲ.实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为_______ 。
(5)高纯度的MnOOH转化为Mn2O3的化学方程式为_______ 。
(6)在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀。请计算使溶液中Al3+完全沉淀需调节pH的最小值为_______ (当溶液中某离子浓度c≤1.0×10-5mol·L-1时,可认为该离子沉淀完全)。

①25℃时相关物质的Ksp见下表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
②氢氧化氧锰(MnOOH)难溶于水和碱性溶液;“沉淀池Ⅰ”的条件下,Co2+不能被二氧化锰氧化。
(1)为提高“酸浸”的效率,可以采取的措施为
(2)向“沉淀池Ⅰ”中加入MnO2,MnO2的作用是
(3)MnSO4转化为MnOOH的离子方程式为
(4)MnSO4转化为MnOOH中“Ⅲ.实验操作”包含过滤、洗涤、干燥。检验MnOOH是否洗涤干净,具体操作为
(5)高纯度的MnOOH转化为Mn2O3的化学方程式为
(6)在“沉淀池Ⅰ”中,滴加氨水调节溶液的pH,使溶液中铝、铁元素完全沉淀。请计算使溶液中Al3+完全沉淀需调节pH的最小值为
Mn2O3是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有少量FeCO3、CoO、Al2O3、SiO2等)为原料制备Mn2O3的工艺流程如图。
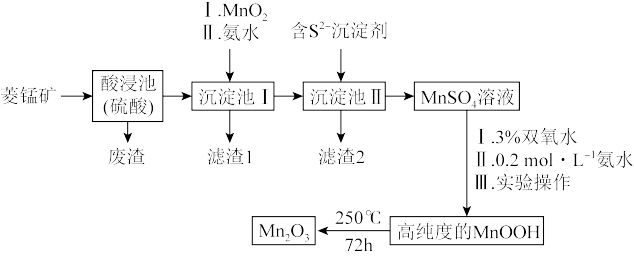
已知:①25℃时相关物质的Ksp见下表。
②氢氧化氧锰(MnOOH)难溶于水和碱性溶液:“沉淀池I”的条件下,Co2+不能被二氧化锰氧化。
回答下列问题:
(1)MnOOH中Mn的化合价为_______ 价。
(2)为提高“酸浸”的效率,可以采取的措施为_______ 。(写一种)
(3)向“沉淀池I”中加入MnO2,MnO2的作用是_______ ;“滤渣2”的主要成分是_______ (填化学式)。
(4)MnSO4转化为MnOOH的离子方程式为_______ 。
(5)在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中Al3+完全沉淀,则理论上pH的最小值为_______ (当溶液中某离子浓度c≦1.0×10-5mol·L-l时,可认为该离子沉淀完全)。

已知:①25℃时相关物质的Ksp见下表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 | Co(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 | 1.09×10-15 |
回答下列问题:
(1)MnOOH中Mn的化合价为
(2)为提高“酸浸”的效率,可以采取的措施为
(3)向“沉淀池I”中加入MnO2,MnO2的作用是
(4)MnSO4转化为MnOOH的离子方程式为
(5)在“沉淀池I”中,滴加氨水调节溶液的pH,使溶液中Al3+完全沉淀,则理论上pH的最小值为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


