解答题-工业流程题 适中0.65 引用2 组卷138
硫酸镍( ,易溶于水)是一种重要的化工原料,主要应用于石油化工、机械制造、医药、动力电池制造及电镀等行业领域中.利用铜冶炼过程中产生的副产物粗硫酸镍制备
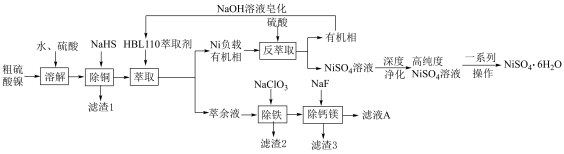
,易溶于水)是一种重要的化工原料,主要应用于石油化工、机械制造、医药、动力电池制造及电镀等行业领域中.利用铜冶炼过程中产生的副产物粗硫酸镍制备 的工艺流程如下:
的工艺流程如下: 等多种离子;
等多种离子; ,离子浓度
,离子浓度 即可认为沉淀完全.
即可认为沉淀完全.
回答下列问题:
(1)“滤渣1”的主要成分是________ (写化学式);
(2)NaHS作“除铜”沉淀剂的缺点是_______ ;
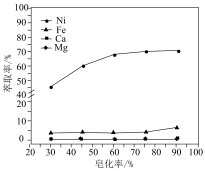
(3)对萃取剂进行皂化是一种强化萃取的常见方法,“萃镍”时加入HBL110萃取剂的同时加入NaOH溶液对萃取剂进行皂化,可以提高镍萃取率,从平衡移动的角度分析原因_____________ .萃取剂皂化率对金属阳离子的萃取率影响如图所示,皂化率最佳取值为_________ .结合图中信息分析,实际生产中将“滤液A”返回至“萃取”工序的原因为__________________ ; ],“除铁”的离子方程式为
],“除铁”的离子方程式为________ ;
(5)若溶液中 ,“除
,“除 ”时,缓慢滴加NaF溶液,则先产生的沉淀1是
”时,缓慢滴加NaF溶液,则先产生的沉淀1是________ (填化学式),当 开始共沉淀时,溶液中“沉淀1”是否沉淀完全?
开始共沉淀时,溶液中“沉淀1”是否沉淀完全?____________ (填“是”或“否”);
(6)滴定法测定 产品中镍元素含量:取3.00g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中,滴入几滴紫脲酸胺指示剂,用浓度为
产品中镍元素含量:取3.00g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中,滴入几滴紫脲酸胺指示剂,用浓度为 的
的 标准液滴定,重复操作2~3次,平均消耗
标准液滴定,重复操作2~3次,平均消耗 标准液17.60mL;
标准液17.60mL;
已知:ⅰ. ;ⅱ.紫脲酸胺:紫色试剂,遇
;ⅱ.紫脲酸胺:紫色试剂,遇 显橙黄色。
显橙黄色。
①滴定至终点时溶液颜色变化为___________ ;
②样品中镍元素的质量分数为__________ %(保留3位有效数字)。
②HBL110萃取剂是由酯类有机物B与磺酸类有机物HA按一定比例混合组成,萃取原理为:
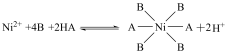 ;
;
回答下列问题:
(1)“滤渣1”的主要成分是
(2)NaHS作“除铜”沉淀剂的缺点是
(3)对萃取剂进行皂化是一种强化萃取的常见方法,“萃镍”时加入HBL110萃取剂的同时加入NaOH溶液对萃取剂进行皂化,可以提高镍萃取率,从平衡移动的角度分析原因
(5)若溶液中
(6)滴定法测定
已知:ⅰ.
①滴定至终点时溶液颜色变化为
②样品中镍元素的质量分数为
2024·河北衡水·模拟预测
类题推荐
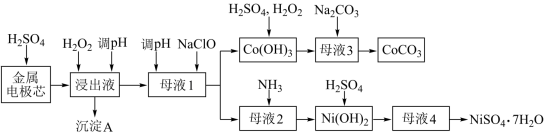
镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯(主要成分为 Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等)生产硫酸镍、碳酸钴工艺流程如下图:
已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表:
回答下列问题:
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有_______ (写出一种合理方法即可),向 Co(OH)3 中加入H2O2 的目的是_______ 。
(2)沉淀 A 的主要成分是_______ (填化学式),“浸出液”调节 pH 的范围为_______ 。
(3)“母液3”中控制Na2CO3用量使终点pH 为9.5,此时c(Co2+)小于_______ mol∙L-1(已知:Ksp[Co(OH)2]=1.6×10-15)。
(4)用滴定法测定 NiSO4∙7H2O 产品中镍元素含量。取 2.00g 样品,酸溶后配成 100mL 溶液,取 20.00mL 于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为 0.100mol∙L-1 的 Na2H2Y 标准液滴定,重复操作2~3 次,消耗 Na2H2Y 标准液平均值为 12.40mL。
已知:i. Ni2++H2Y2-=[NiY]2-+2H+;ii. 紫脲酸胺:紫色试剂,遇 Ni2+显橙黄色。
①滴定至终点的现象是_______ ;②样品中镍元素的质量分数为_______ %(保留 3 位有效数字)。
(5)NiSO4 在强碱溶液中和 NaClO 反应,可制得碱性镍镉电池电极材料 NiOOH,该反应的离子方程式为_______ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时 pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时 pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.15 |
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有
(2)沉淀 A 的主要成分是
(3)“母液3”中控制Na2CO3用量使终点pH 为9.5,此时c(Co2+)小于
(4)用滴定法测定 NiSO4∙7H2O 产品中镍元素含量。取 2.00g 样品,酸溶后配成 100mL 溶液,取 20.00mL 于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为 0.100mol∙L-1 的 Na2H2Y 标准液滴定,重复操作2~3 次,消耗 Na2H2Y 标准液平均值为 12.40mL。
已知:i. Ni2++H2Y2-=[NiY]2-+2H+;ii. 紫脲酸胺:紫色试剂,遇 Ni2+显橙黄色。
①滴定至终点的现象是
(5)NiSO4 在强碱溶液中和 NaClO 反应,可制得碱性镍镉电池电极材料 NiOOH,该反应的离子方程式为
镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯(主要成分为Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等)生产硫酸镍、碳酸钴工艺流程如下图:
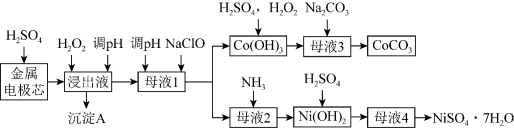
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有______ (写出一种合理方法即可),向Co(OH)3中加入H2O2的目的是_______ 。
(2)沉淀A的主要成分是_______ (填化学式),“浸出液”调节pH的范围为________ 。
(3)“母液3”中控制Na2CO3用量使终点pH为9.5,此时c(Co2+)小于________ mol∙L-1(已知:Ksp[Co(OH)2]=1.6×10-15)。
(4)用滴定法测定NiSO4∙7H2O产品中镍元素含量。取2.00g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100mol∙L-1的Na2H2Y标准液滴定,重复操作2~3次,消耗Na2H2Y标准液平均值为12.40mL。
已知:i.Ni2++H2Y2-=[NiY]2-+2H+
ii.紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的操作和现象是_______ 。
②样品中镍元素的质量分数为_______ %(精确到0.01)。
(5)NiSO4在强碱溶液中和NaClO反应,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为_______ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.15 |
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有
(2)沉淀A的主要成分是
(3)“母液3”中控制Na2CO3用量使终点pH为9.5,此时c(Co2+)小于
(4)用滴定法测定NiSO4∙7H2O产品中镍元素含量。取2.00g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为0.100mol∙L-1的Na2H2Y标准液滴定,重复操作2~3次,消耗Na2H2Y标准液平均值为12.40mL。
已知:i.Ni2++H2Y2-=[NiY]2-+2H+
ii.紫脲酸胺:紫色试剂,遇Ni2+显橙黄色。
①滴定终点的操作和现象是
②样品中镍元素的质量分数为
(5)NiSO4在强碱溶液中和NaClO反应,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为
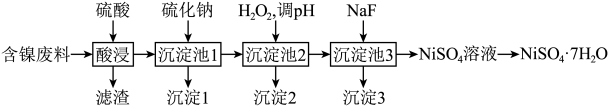
镍是一种常用催化剂。某工厂采用以下流程提取含镍废料(主要含Ni、NiO,以及少量CuO、FeO、 、MgO、ZnO、
、MgO、ZnO、 和
和 等)中的镍,实现资源再利用。
等)中的镍,实现资源再利用。 和
和
常温下,某些金属离子形成氢氧化物开始沉淀和完全沉淀的pH:
回答下列问题:
(1)NiO中 的核外电子排布式为
的核外电子排布式为___________ 。
(2)为提高酸浸率,可采取的措施有___________ (写出两项即可)。
(3)当 、
、 完全沉淀时,溶液中
完全沉淀时,溶液中 浓度至少应为
浓度至少应为___________ (常温下,当溶液中的离子浓度小于 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(4)沉淀池2中加入 的目的是
的目的是___________ (用离子方程式表示),为使相应离子完全沉淀,沉淀池2的pH范围应控制在___________ 。
(5)沉淀3的成分是___________ (填化学式)。
(6)用滴定法测定 产品中镍元素含量。取2.000g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入紫脲酸胺指示剂,用浓度为0.100mol/L的
产品中镍元素含量。取2.000g样品,酸溶后配成100mL溶液,取20.00mL于锥形瓶中进行滴定,滴入紫脲酸胺指示剂,用浓度为0.100mol/L的 标准液滴定,重复操作2~3次,消耗
标准液滴定,重复操作2~3次,消耗 标准液平均值为12.40mL。(已知:ⅰ.
标准液平均值为12.40mL。(已知:ⅰ. ;ⅱ.紫脲酸胺:紫色试剂,遇
;ⅱ.紫脲酸胺:紫色试剂,遇 显橙黄色。)
显橙黄色。)
①滴定至终点的现象是___________ 。
②样品中镍元素的质量分数为___________ (保留4位有效数字)。
常温下,某些金属离子形成氢氧化物开始沉淀和完全沉淀的pH:
| 金属离子 | |||||
| 开始沉淀的pH | 2.3 | 6.8 | 3.5 | 8.6 | 7.1 |
| 完全沉淀的pH | 3.2 | 8.3 | 4.6 | 11.1 | 9.0 |
(1)NiO中
(2)为提高酸浸率,可采取的措施有
(3)当
(4)沉淀池2中加入
(5)沉淀3的成分是
(6)用滴定法测定
①滴定至终点的现象是
②样品中镍元素的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


