解答题-原理综合题 较难0.4 引用1 组卷91
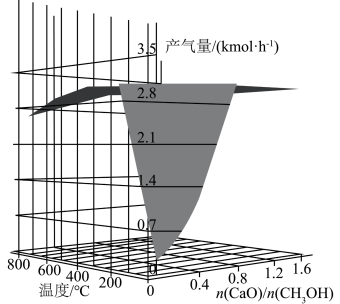
作为新质生产力培育的重要领域,目前氢能发展正处在提质增效的关键阶段。甲醇水蒸气重整制氢的方法是目前比较成熟的制氢方法,其部分反应过程如图1所示:_______ kJ⋅mol⁻¹,该条件下反应Ⅲ的热化学方程式为_______ 。
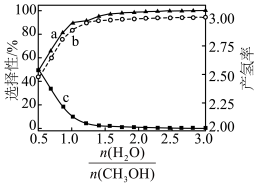
(2)下图为T℃平衡时含碳产物的选择性(如CO的选择性是指反应生成CO的甲醇占转化的甲醇的百分比)及产氢率 随水醇比
随水醇比 的变化图像如图2,曲线
的变化图像如图2,曲线_______ (填“a”、“b”或“c”)是CO的选择性曲线。由图2可知,工业生产中最优水醇比暴_______ (填序号)。
(3)甲醇水蒸气重整反应是在吸附剂CaO存在的情况下进行的,已知吸附剂CaO的碳酸化反应为: ,T℃时,
,T℃时,  在温度为T℃的恒压容器的石英管中加入适量CaO,按
在温度为T℃的恒压容器的石英管中加入适量CaO,按  通入水蒸气和甲醇,测得压强为P₀kPa,,反应平衡时氢气的分压为b kPa,若此时氧化钙对二氧化碳的吸收率为50%,则CO₂的平衡分压为
通入水蒸气和甲醇,测得压强为P₀kPa,,反应平衡时氢气的分压为b kPa,若此时氧化钙对二氧化碳的吸收率为50%,则CO₂的平衡分压为_______ kPa,反应I的Kₚ₁=_______ 。若继续加入甲醇反应至新平衡,与原平衡相比
_______ (填“增大”“减小”或“不变”)

(2)下图为T℃平衡时含碳产物的选择性(如CO的选择性是指反应生成CO的甲醇占转化的甲醇的百分比)及产氢率

(3)甲醇水蒸气重整反应是在吸附剂CaO存在的情况下进行的,已知吸附剂CaO的碳酸化反应为:
2024·山东泰安·模拟预测
类题推荐
碳和碳的化合物在生产、生活中有重要作用,乙烯、甲醇、甲酸等都是重要的能源物质。
(1)已知几种反应的正反应活化能(E1)、逆反应活化能(E2)如表所示:
在相同条件下,起始反应最快的是_____ (填序号)。 的
的
_____ 。
(2)甲醇水蒸气重整,总反应为 。
。
①若工业生产中在恒压容器中进行该反应,下列措施可提高CH3OH的平衡转化率的是_____ (填字母)。
a.原料气中掺入一定量惰性气体
b.升高温度
c.使用催化效率更高的催化剂
d.使用分子筛及时移走产生的氢气
②该过程中同时发生两个反应:
I.
Ⅱ.
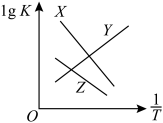
总反应、反应Ⅰ、反应Ⅱ的平衡常数对数lgK与 变化关系如图所示。图中X和Y、Z三条曲线中,表示反应Ⅰ的是
变化关系如图所示。图中X和Y、Z三条曲线中,表示反应Ⅰ的是_____ ,理由是_____ 。
③在恒容密闭容器中,充入一定量CH3OH(g)和H2O(g),同时发生反应Ⅰ、反应Ⅱ,实验测得不同温度下,平衡体系中H2的体积分数如图所示:
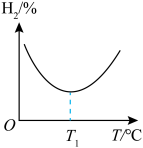
T1°C之后平衡体系中H2体积分数增大的原因是_____ 。
(3)CO2催化还原可以制备 和HCOOH:
和HCOOH:
 ;
;
 。
。
在一定温度下,在容积为1L的恒容密闭容器中充入1molCO2(g)和3molH2(g),同时发生了乙烯化和甲酸化反应,达到平衡时C2H4的选择性为40%,体系压强减小了22.5%。则CO2总转化率为_____ ,该温度下,甲酸化的平衡常数K=_____ (结果保留2位小数)。提示:
(1)已知几种反应的正反应活化能(E1)、逆反应活化能(E2)如表所示:
| 序号 | 化学反应 | E1/(kJ·mol-¹) | E2/(kJ·mol-¹) |
| ① | 1954 | 2519 | |
| ② | 685 | 970 | |
| ③ | 3526 | 4978 |
(2)甲醇水蒸气重整,总反应为
①若工业生产中在恒压容器中进行该反应,下列措施可提高CH3OH的平衡转化率的是
a.原料气中掺入一定量惰性气体
b.升高温度
c.使用催化效率更高的催化剂
d.使用分子筛及时移走产生的氢气
②该过程中同时发生两个反应:
I.
Ⅱ.
总反应、反应Ⅰ、反应Ⅱ的平衡常数对数lgK与

③在恒容密闭容器中,充入一定量CH3OH(g)和H2O(g),同时发生反应Ⅰ、反应Ⅱ,实验测得不同温度下,平衡体系中H2的体积分数如图所示:

T1°C之后平衡体系中H2体积分数增大的原因是
(3)CO2催化还原可以制备
在一定温度下,在容积为1L的恒容密闭容器中充入1molCO2(g)和3molH2(g),同时发生了乙烯化和甲酸化反应,达到平衡时C2H4的选择性为40%,体系压强减小了22.5%。则CO2总转化率为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网