多选题 较难0.4 引用1 组卷84
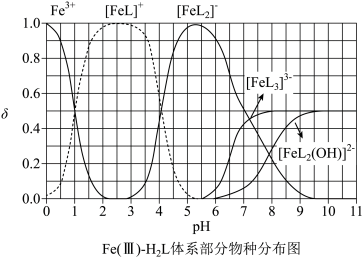
H₂L为某邻苯二酚类配体,其pKa1=7.46,pK2=12.4(pKa=-lgKa)。常温下构建Fe(Ⅲ)-H₂I溶液体系,其中c0(Fe3+)=2.0×10-4mol·L,c0(H2L)=5.0×10-3mol⋅L-1。体系中含Fe物种的组分分布系数δ与pH的关系如图所示,分布系数  ,已知lg 5≈0.7。下列说法正确的是
,已知lg 5≈0.7。下列说法正确的是
| A.当pH=0.5时,体系中c(H2L)>c([FeL]+)>c(OH-)>c(HL-) |
| B.L²⁻+Fe³⁺ |
| C.pH在9.5~10.5之间,含L的物种主要为HL⁻ |
| D.当pH=10时,参与配位的c(L²⁻)≈2×10⁻⁴mol⋅L⁻¹ |
2024·山东泰安·模拟预测
类题推荐  为某邻苯二酚类配体,其
为某邻苯二酚类配体,其 ,
, 。常温下构建
。常温下构建 溶液体系,其中
溶液体系,其中 ,
, 。体系中含Fe物种的组分分布系数
。体系中含Fe物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数 ,已知
,已知 ,
, 。下列说法正确的是
。下列说法正确的是


| A.当pH=a时,体系中 |
| B.当pH=8.5时,参与配位的 |
| C. |
| D.当pH=10时, |
已知丙二酸(HOOCCH2COOH,简记为H2A)是二元弱酸。常温下,向20.0 mL0.1 mol·L-1丙二酸溶液中滴加同浓度的NaOH溶液V mL,体系中含碳粒子的物质的量分布系数(δ)与pH的关系如图所示。已知:丙二酸在体系中物质的量分布系数为δ(H2A)=  。
。

下列叙述正确的是

下列叙述正确的是
| A.V=20.0时,c(HA-)>c(H2A)>c(A2- ) |
| B.b点对应的溶液温度为滴定过程中的最高值 |
| C.V=40.0时,c(H2A)+c(HA- )+c(A2-)=0.1 mol ·L-1 |
| D.常温下,H2A+A2- |
室温下,向10mL 0.1mol/L的H2SO3溶液中滴加0.1mol/L的NaOH溶液,各含硫微粒分布系数(平衡时某微粒的物质的量占各微粒物质的量之和的分数)与溶液pH的关系如图所示。下列说法不正确 的是

| A.曲线Ⅱ表示HSO |
| B.Ka2(H2SO3)的数量级为10−8 |
| C.pH=7时,c(Na+)<3c(SO |
| D.当加入的NaOH的体积为20mL时,c(H+)+ c(HSO |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


