解答题-原理综合题 较难0.4 引用1 组卷66
2020年9月22日,国家主席习近平在第七十五届联合国大会上宣布:“中国力争在2030年前 排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是
排放达到峰值,努力争取2060年前实现碳中和目标。”中国科学院马延和团队发表于Science上的论文成果显示:实验室条件下,只需4个小时11步就能合成淀粉,其中关键步骤是 转化为甲醇:
转化为甲醇: 。
。
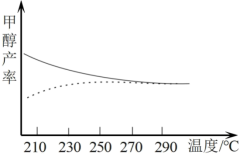
【小题1】现研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中 和
和 的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是
的投料比不变,得到甲醇实际产率、平衡产率与温度的关系如图,图中实线代表的是___________ 。
【小题2】由此判断
___________ 0(填“>”、“=”或“<”),请分别阐述你做出上述实线选择和判断 的依据
的依据___________ 。
【小题3】该反应的自发条件是___________ 。
A.高温自发 B.低温自发 C.任何温度下都自发
【小题4】恒温恒容条件下,有利于提高 的平衡转化率的措施有
的平衡转化率的措施有
【小题5】向恒温恒容容器中投入2mol  和等量
和等量 ,下列能说明该反应已达平衡状态的是
,下列能说明该反应已达平衡状态的是
 除了能转化为
除了能转化为 外,还可以和
外,还可以和 反应生成CO:
反应生成CO:
其化学平衡常数和温度的关系如下表所示:
【小题6】某温度下,平衡浓度符合 ,此时温度介于___________范围。
,此时温度介于___________范围。
【小题7】在820℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为: 、
、 、
、 、
、 ,则下一时刻,反应向___________进行。
,则下一时刻,反应向___________进行。
【小题1】现研究温度对于甲醇产率的影响。在210℃~290℃,保持原料气中
【小题2】由此判断
【小题3】该反应的自发条件是
A.高温自发 B.低温自发 C.任何温度下都自发
【小题4】恒温恒容条件下,有利于提高
| A.使用催化剂 | B.加压 |
| C.减小 | D.平衡后,同等比例的增加反应物的量 |
| A. | B.气体的密度不再变化 |
| C.混合气体的平均摩尔质量不再变化 | D. |
其化学平衡常数和温度的关系如下表所示:
| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A.<700℃ | B.700-800℃ | C.1000-1200℃ | D.无法判断 |
| A.正向 | B.逆向 | C.不移动 | D.无法判断 |
23-24高三下·上海·阶段练习
类题推荐
2020年9月22日,国家主席习近平在第七十五届联合国大会一般性辩论上发表重要讲话时指出,中国将采取有力的政策和措施,力争于2030年前二氧化碳排放达到峰值,努力争取2060年前实现碳中和。为此,科学家们正在努力探索 资源化技术。
资源化技术。
方法1:近年我国大力加强温室气体 催化氢化合成甲醇技术的工业化研究,实现可持续发展。涉及反应如下:
催化氢化合成甲醇技术的工业化研究,实现可持续发展。涉及反应如下:




(1)写出利用 和
和 合成甲醇的热化学方程式
合成甲醇的热化学方程式___________ ;判断上述反应能自发进行的条件是___________ 。
(2)在一定温度下,向2L密闭容器中加入2mol 、6mol
、6mol  ,在适当的催化剂作用下,发生反应:
,在适当的催化剂作用下,发生反应: ,下列叙述能说明此反应一定达到平衡状态的是
,下列叙述能说明此反应一定达到平衡状态的是___________
A.混合气体的平均相对分子质量保持不变B. 和
和 的转化率相等
的转化率相等
C.混合气体的密度保持不变D.有3mol H-O键生成的同时有3mol H-H键生成
(3)250℃时,在恒容密闭容器中由 (g)催化氢化合成
(g)催化氢化合成 ,不同投料比
,不同投料比 时某反应物X的平衡转化率变化曲线如图所示。反应物X是
时某反应物X的平衡转化率变化曲线如图所示。反应物X是___________ (填“ ”或“
”或“ ”),判断依据是
”),判断依据是___________ 。
(4)催化剂和反应条件与反应物转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,四组实验数据如下表所示:
根据上表所给数据,用 生产甲醇的最优选项为
生产甲醇的最优选项为___________ (填字母)。
方法2:用二氧化碳催化加氢还可用来合成低碳烯烃。
反应开始时,在体积为0.1L的密闭容器中,初始充入 的物质的量为0.3mol,
的物质的量为0.3mol, 的物质的量为0.1mol,发生反应:
的物质的量为0.1mol,发生反应: ,不同温度下平衡时的四种气态物质的物质的量百分数如图所示:
,不同温度下平衡时的四种气态物质的物质的量百分数如图所示:

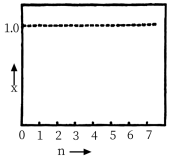
(5)在120℃达到平衡时,此温度下的平衡常数为___________ (用分数表示)。若氢气和二氧化碳的物质的量之比为 进行投料,温度控制为120℃,相应平衡体系中乙烯的产率为x,在上图中绘制x随n(
进行投料,温度控制为120℃,相应平衡体系中乙烯的产率为x,在上图中绘制x随n( )变化的示意图(标出曲线的起点坐标)
)变化的示意图(标出曲线的起点坐标)___________ 。
方法1:近年我国大力加强温室气体
(1)写出利用
(2)在一定温度下,向2L密闭容器中加入2mol
A.混合气体的平均相对分子质量保持不变B.
C.混合气体的密度保持不变D.有3mol H-O键生成的同时有3mol H-H键生成
(3)250℃时,在恒容密闭容器中由
(4)催化剂和反应条件与反应物转化率和产物的选择性高度相关。控制相同投料比和相同反应时间,四组实验数据如下表所示:
| 实验编号 | 温度(K) | 催化剂 | 甲醇选择性(%) | |
| A | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
| B | 543 | Cu/ZnO纳米片 | 11.9 | 72.7 |
| C | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
| D | 553 | Cu/ZnO纳米片 | 12.0 | 70.6 |
根据上表所给数据,用
方法2:用二氧化碳催化加氢还可用来合成低碳烯烃。
反应开始时,在体积为0.1L的密闭容器中,初始充入


(5)在120℃达到平衡时,此温度下的平衡常数为
为减少温室效应,可将CO2转化成其它可燃物质,如CH3OH等。探究CO2合成CH3OH的反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:I.CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1=-48.5kJ•mol-1
II.CO(g)+2H2(g)=CH3OH(g) △H2=-92.4kJ•mol-1
Ⅲ.CO2(g)+H2(g)=CO(g)+H2O(g) △H3
回答下列问题:
(1)△H3=__ kJ•mol-1。
(2)已知:在一恒温、恒容密闭容器中充入1molCO2和3molH2,一定条件下发生反应I,测得CO2和CH3OH(g)的浓度随时间变化如图所示。请回答:
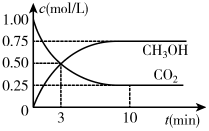
①达到平衡的时刻是__ min(填“3”或“10”)。
②能判断该反应达到化学平衡状态的依据是__ 。
a.容器压强不变
b.混合气体的平均摩尔质量不变
c.v(CH3OH)=v(H2O)
d.c(CH3OH)=c(H2O)
③为了提高H2的转化率,可采取__ (填“增大”或“减小”)CO2浓度的措施。
④该反应的平衡常数K=__ 。
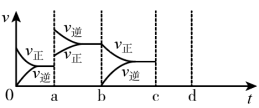
⑤如图表示在密闭容器中上述反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是__ ;b时改变的条件可能是__ 。
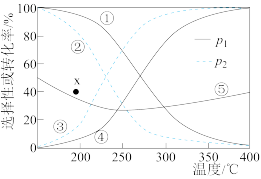
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,发生反应I、Ⅱ、Ⅲ,回答下列实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。
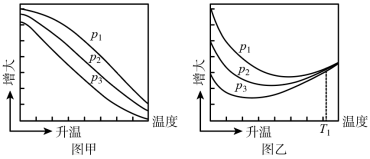
其中纵坐标表示CO2平衡转化率的是图__ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为__ ;图乙中T1温度时,三条曲线几乎交于一点的原因是__ 。
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为__ (填字母代号)。
(5)在一固定容积的密闭容器中进行反应Ⅲ:CO2(g)+H2(g) CO(g)+H2O(g),当温度为850℃时,K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见表:
CO(g)+H2O(g),当温度为850℃时,K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见表:
①此时上述的反应中正、逆反应速率的关系式是__ (填代号)。
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
②在700℃通过压缩体积增大气体压强,则该反应中H2(g)的转化率__ (“增大”、“减小”或“不变”);工业生产中,通过此方法使容器内气体压强增大以加快反应,却意外发现H2(g)的转化率也显著提高,请你从平衡原理解释其可能原因是:__ 。
II.CO(g)+2H2(g)=CH3OH(g) △H2=-92.4kJ•mol-1
Ⅲ.CO2(g)+H2(g)=CO(g)+H2O(g) △H3
回答下列问题:
(1)△H3=
(2)已知:在一恒温、恒容密闭容器中充入1molCO2和3molH2,一定条件下发生反应I,测得CO2和CH3OH(g)的浓度随时间变化如图所示。请回答:

①达到平衡的时刻是
②能判断该反应达到化学平衡状态的依据是
a.容器压强不变
b.混合气体的平均摩尔质量不变
c.v(CH3OH)=v(H2O)
d.c(CH3OH)=c(H2O)
③为了提高H2的转化率,可采取
④该反应的平衡常数K=
⑤如图表示在密闭容器中上述反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是

(3)不同压强下,按照n(CO2):n(H2)=1:3投料,发生反应I、Ⅱ、Ⅲ,回答下列实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图
(4)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为
| A.高温、高压 | B.高温、低压 | C.低温、高压 | D.低温、低压 |
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
①此时上述的反应中正、逆反应速率的关系式是
A.v(正)>v(逆) B.v(正)<v(逆) C.v(正)=v(逆) D.无法判断
②在700℃通过压缩体积增大气体压强,则该反应中H2(g)的转化率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网