单选题 适中0.65 引用5 组卷268
电化学中,常用电极电势表示一定条件下微粒得失电子能力,电极电势越高氧化性越强。标准状态下,氧化型电极反应 ,
, ,
, ,则
,则 的氧化性比
的氧化性比 强。含钴微粒的电极电势随
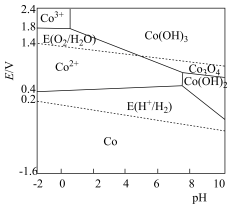
强。含钴微粒的电极电势随 的变化如图所示,两条虚线分别表示“氧线”和“氢线”。下列说法错误的是
的变化如图所示,两条虚线分别表示“氧线”和“氢线”。下列说法错误的是
| A.单质 |
| B.氧气的氧化性与溶液的酸碱性有关 |
| C.一定条件下 |
| D.酸性条件下,反应 |
2024·山东·模拟预测
类题推荐
在常温下,发生下列几个反应:
①2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②Cl2+2NaBr=2NaCl+Br2
③Br2+2FeBr2=2FeBr3
根据上述反应,下列结论正确的是
①2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②Cl2+2NaBr=2NaCl+Br2
③Br2+2FeBr2=2FeBr3
根据上述反应,下列结论正确的是
| A.还原性强弱顺序为:Br->Fe2+>Cl- |
| B.氧化性强弱顺序为:MnO |
| C.溶液中可发生反应:2Fe3++2Cl-=2Fe2++Cl2↑ |
| D.反应①中,氧化剂与还原剂的个数之比为1:8 |
已知反应:2FeCl3+2KI=2FeCl2+I2+2KCl,H2S+I2=S+2HI,2FeCl2+Cl2=2FeCl3,由此得出下列微粒氧化性由强到弱的顺序为
| A.Cl2 > I2> Fe3+ > S | B.Cl2 > Fe3+ > I2 > S |
| C.Fe3+ > Cl2 > I2 > S | D.S > I2 > Fe3+ > Cl2 |
高铁酸钾(K2FeO4)是一种高效绿色水处理剂,其工业制备的反应原理为: 2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+5H2O。下列说法错误的是
| A.氧化剂是KClO,还原剂是Fe(OH)3 |
| B.Fe(OH)3发生氧化反应 |
| C.氧化性:K2FeO4>KClO |
| D.KClO具有氧化性 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


