解答题-原理综合题 较难0.4 引用1 组卷52
回答下列问题:
(1)已知 时在某恒容密闭容器中加入足量的
时在某恒容密闭容器中加入足量的 和
和 发生如下几个反应:
发生如下几个反应:









①写出基态 原子的价层电子排布图:
原子的价层电子排布图:_______ 。
②
_______ (用含 、
、 代数式表示)。
代数式表示)。
③若上述反应达到平衡后 的转化率为
的转化率为 ,经检测体系中含有
,经检测体系中含有 ,则得到
,则得到_______  金属铁。若再加入一定量的
金属铁。若再加入一定量的 ,再次达到平衡后,
,再次达到平衡后, 的值将
的值将_______ (填标号)。
A.增大 B.减小 C.不变 D.无法确定
(2)通过下列反应可实现 的再转化,合成
的再转化,合成 、
、 :
:
①

②

在密闭容器中通入一定量的 和
和 ,分别在压强为
,分别在压强为 和
和 下进行反应。实验中对平衡体系的三种物质(
下进行反应。实验中对平衡体系的三种物质( 、
、 、
、 )进行分析,其中温度对
)进行分析,其中温度对 和
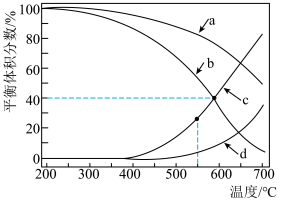
和 在三种物质中的体积分数影响如图所示。
在三种物质中的体积分数影响如图所示。 时
时 平衡体积分数随温度变化关系的曲线是
平衡体积分数随温度变化关系的曲线是_______ (填“a”“b”“o”或“d”中的一种)。简述理由:_______ 。
(3)有一个经验规则可以用于估算基元反应的活化能 :
:
(BE:反应中断掉的化学键的键能之和)
①反应中没有化学键断裂的反应;②自由基与分子的放热反应;③反应中化学键不完全断裂(如协同反应)的反应;④反应中化学键完全断裂的反应。
根据上述经验规则,估算氢气与氯气生成氯化氢的反应历程中第ⅱ步基元反应的活化能
_______ ,并与实验值 比较。
比较。
ⅰ.

ⅱ.

ⅲ.

ⅳ.

 ;
; ;
;

上述反应历程中决定整个反应的速率是第_______ (填标号)步反应。
(1)已知
①写出基态
②
③若上述反应达到平衡后
A.增大 B.减小 C.不变 D.无法确定
(2)通过下列反应可实现
①
②
在密闭容器中通入一定量的
(3)有一个经验规则可以用于估算基元反应的活化能
反应类型 | ① | ② | ③ | ④ |
| 0 | 0.05 | 0.3 | 1 |
①反应中没有化学键断裂的反应;②自由基与分子的放热反应;③反应中化学键不完全断裂(如协同反应)的反应;④反应中化学键完全断裂的反应。
根据上述经验规则,估算氢气与氯气生成氯化氢的反应历程中第ⅱ步基元反应的活化能
ⅰ.
ⅱ.
ⅲ.
ⅳ.
上述反应历程中决定整个反应的速率是第
2024·全国·模拟预测
类题推荐  重整反应【
重整反应【
 】可以生成合成气。如何减少反应过程中的积炭,是研究的热点之一、某条件下,发生主反应的同时,还发生了积炭反应:
】可以生成合成气。如何减少反应过程中的积炭,是研究的热点之一、某条件下,发生主反应的同时,还发生了积炭反应:
 歧化:
歧化:

 裂解:
裂解:

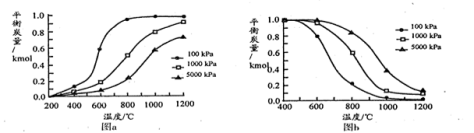
(1)对上述两个积炭反应分别进行计算,得到以下温度和压强对积炭反应中平衡炭量的影响图,其中表示温度和压强对 裂解反应中平衡炭量影响的是
裂解反应中平衡炭量影响的是___________ (填“图a”或“图b”),
___________ 0(填“>”或“<”),___________ (填“高温”或“低温”)有利于 歧化反应自发进行。
歧化反应自发进行。
(2)实验表明,在重整反应中,为抑制积炭产生,应选用高温、低压条件,由此可推断,该重整反应过程中的积炭主要由___________ 反应产生。
(3)一定条件下, 裂解的反应历程如图所示。该历程分
裂解的反应历程如图所示。该历程分___________ 步进行,其中决定 裂解反应快慢的基元反应
裂解反应快慢的基元反应___________ (写出化学方程式)。

(4)同温下,某研究小组分别在容积相等的两个恒容密闭容器中加入一定量的反应物,控制反应条件使其仅发生 重整反应,获得如下效据:
重整反应,获得如下效据:
①容器ⅰ中反应达到平衡时,生成 的物质的量为
的物质的量为___________ ,容器ⅱ中反应达到平衡状态过程中吸收的热量___________ ,247kJ(填“>”、“<”或“=”)。
②容器ⅰ的容积变为原来的一半,则 平衡转化率
平衡转化率___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③计算容器ⅱ中反应的平衡常数
___________  (用平衡分压代替平衡浓度计算,分压
(用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)。
物质的量分数)。
将玉米秸秆进行热化学裂解可制备出以CO、 、
、 、
、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
(1)已知:几种常见共价键的键能如下表所示。
由此可估算反应 的焓变
的焓变
_______  。
。
(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是_______(填标号)。
(3) 和
和 合成乙醇的反应为
合成乙醇的反应为 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时
充入一刚性容器中,测得平衡时 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。
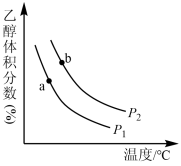
①压强
_______  (填“>”“<”或“=”,下同)。判断依据是
(填“>”“<”或“=”,下同)。判断依据是_______ 。
②a、b两点的平衡常数
_______  。
。
③已知Arrhenius经验公式为 (Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea=_______  。从图中信息获知催化效能较高的催化剂是
。从图中信息获知催化效能较高的催化剂是_______ (填“m”或“n”)。

(1)已知:几种常见共价键的键能如下表所示。
| 共价键 | C—H | C—O | H—H | O—H | |
| 键能( | 413 | 358 | 839 | 436 | 467 |
(2)若在恒容绝热的密闭容器中进行上述反应,下列说法正确的是_______(填标号)。
| A.体系温度不再发生变化时,反应达到化学平衡状态 |
| B.平衡体系中, |
| C.加入催化剂,可以提高 |
| D.其他条件不变,增大CO的浓度,能提高 |

①压强
②a、b两点的平衡常数
③已知Arrhenius经验公式为


(1)对上述两个积炭反应分别进行计算,得到以下温度和压强对积炭反应中平衡炭量的影响图,其中表示温度和压强对
(2)实验表明,在重整反应中,为抑制积炭产生,应选用高温、低压条件,由此可推断,该重整反应过程中的积炭主要由
(3)一定条件下,

(4)同温下,某研究小组分别在容积相等的两个恒容密闭容器中加入一定量的反应物,控制反应条件使其仅发生
| 容器编号 | 起始时各物质的物质的量/mol | 达到平衡时体系的压强/MPa | 达到平衡时体系能量的变化 | ||||
| ⅰ | 1 | 2 | 0 | 0 | P | 吸收热量:123.5kJ | |
| ⅱ | 2 | 4 | 0 | 0 | |||
②容器ⅰ的容积变为原来的一半,则
③计算容器ⅱ中反应的平衡常数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网





