解答题-工业流程题 适中0.65 引用1 组卷74
随着新能源汽车的发展,废旧锂电池需要回收处理。一种对磷酸亚铁锂废电池处理料(主要成分为LiFePO4、FePO4、Al、C等)的回收处理工艺流程如下所示。
(1)已知
 OH-+Al(OH)3,K1=6.25×10-2;
OH-+Al(OH)3,K1=6.25×10-2;
 H++
H++ ,K2=4.7×10-11;“滤液”中的溶质主要是NaAl(OH)4,则步骤①中Al主要反应的离子方程式为
,K2=4.7×10-11;“滤液”中的溶质主要是NaAl(OH)4,则步骤①中Al主要反应的离子方程式为_______ ﹔步骤②曾有学者研究用NaHCO3代替H2SO4,则用NaHCO3溶液反应的平衡常数的数量级为_______ ,当反应平衡常数大于105时,可视为反应完全,则用NaHCO3代替H2SO4的反应是否完全?_______ 。
(2)步骤③硫酸溶液足量,“滤渣2”的成分是_______ ,实际反应中H2O2用量超过理论值,原因是_______ ;试写出Fe2+与H2O2按物质的量1∶1反应的总离子反应方程式:_______ 。
(3)若步骤④处加入NaOH溶液和NH3·H2O溶液后Li+浓度为0.55mol/L,则此处所调pH的范围为_______ 。滤液4的主要阳离子有_______ (填离子符号)。
(4)步骤⑤主要是回收利用_______ 元素。

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH | Ksp(氢氧化物) | Ksp(盐) |
| Fe3+ | 2.24 | 3.2 | 3.2×10-38 | Ksp(FePO4)=1.3×10-22 |
| Li+ | 5.5×10-3 | Ksp(Li2CO3)=1.7×10-3 |
(1)已知
(2)步骤③硫酸溶液足量,“滤渣2”的成分是
(3)若步骤④处加入NaOH溶液和NH3·H2O溶液后Li+浓度为0.55mol/L,则此处所调pH的范围为
(4)步骤⑤主要是回收利用
2024·四川泸州·三模
类题推荐
锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示:
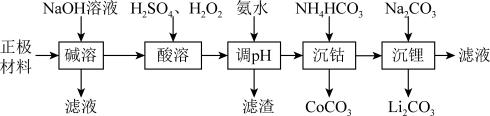
已知:①Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性;
②相关金属离子形成氢氧化物沉淀的pH值如下表所示:
回答下列问题:
(1)写出“碱溶”时发生主要反应的离子方程式:____________________________________ 。
(2)为提高“酸溶”的浸出速率,可采取的措施有___________________________ (任写一种)。
(3)“酸溶”时,LiCoO2发生的主要反应的离子方程式为_____________________________ ;若用浓盐酸代替H2SO4和H2O2的混合液,缺点是___________________________________ 。
(4)用氨水调节pH的范围为____________ ,若“沉钴”后溶液中c(Li+)=4 mol·L-1,加入等体积的Na2CO3溶液后,沉淀中的Li元素占原Li元素总量的90%,则“沉锂”后溶液中c( )=
)=__________ mol·L-1。
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为________________ 。
(6)写出“沉钴”过程中发生反应的离子方程式:____________________________________ 。

已知:①Ksp(Li2CO3)=1.6×10-3,LiCoO2难溶于水,具有强氧化性;
②相关金属离子形成氢氧化物沉淀的pH值如下表所示:
Al3+ | Fe3+ | Fe2+ | Co2+ | |
开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.0 |
回答下列问题:
(1)写出“碱溶”时发生主要反应的离子方程式:
(2)为提高“酸溶”的浸出速率,可采取的措施有
(3)“酸溶”时,LiCoO2发生的主要反应的离子方程式为
(4)用氨水调节pH的范围为
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为
(6)写出“沉钴”过程中发生反应的离子方程式:
锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示:
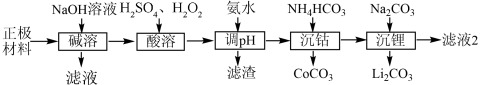
已知:① Ksp(Li2CO3)=1.6 ×10-3, LiCoO2难溶于水,具有强氧化性:
②相关金属离子形成氢氧化物沉淀的pH值如表所示:
回答下列问题:
(1)写出“碱溶”时发生主要反应的离子方程式:___________ 。
(2)“酸溶”时,LiCoO2发生的主要反应的离子方程式为___________ ;用浓盐酸代替H2SO4和H2O2的混合液,缺点是___________ 。
(3)用氨水调节pH的范围为___________ 。
(4)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为___________ 。
(5)写出“沉钴”过程中发生反应的离子方程式:___________ 。

已知:① Ksp(Li2CO3)=1.6 ×10-3, LiCoO2难溶于水,具有强氧化性:
②相关金属离子形成氢氧化物沉淀的pH值如表所示:
| 金属阳离子 | A13+ | Fe3+ | Fe2+ | Co2+ |
| 开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.0 |
(1)写出“碱溶”时发生主要反应的离子方程式:
(2)“酸溶”时,LiCoO2发生的主要反应的离子方程式为
(3)用氨水调节pH的范围为
(4)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为
(5)写出“沉钴”过程中发生反应的离子方程式:
ZnO有优异的常温发光性能,在半导体领域的液晶显示器、薄膜晶体管、发光二极管等产品中均有应用。工业上利用锌焙砂(主要成分为ZnO、ZnFe2O4,还含有Fe3O4、Al2O3、SiO2等)制取氧化锌的工艺流程如图所示:
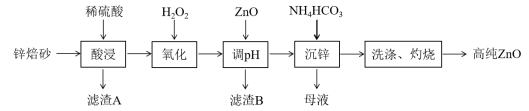
已知:相关金属离子c(Mn+)=0.1 mol·L-1生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)ZnFe2O4可写出ZnO·Fe2O3,则ZnFe2O4与H2SO4反应的化学方程式___________ ;“酸浸”时为了提高浸取速率,可以采取的措施是___________ (任写一种)。
(2)“氧化”步骤中发生的离子方程式为___________ ,H2O2的实际用量比理论用量要大,原因是___________ 。
(3)滤渣B的主要成分为___________ ;加ZnO时,为了不生成Zn(OH)2,该步骤需要控制溶液pH的范围是___________ ;若室温下将溶液的pH调为4,则此时Fe3+的浓度为___________ (已知Ksp[Fe(OH)3]=4×10−38)。
(4)“沉锌”反应中,往滤液加入NH4HCO3溶液,生成ZnCO3·Zn(OH)2及CO2,写出相应的离子方程式___________ 。“沉锌”后的母液可进一步处理,获得一种化工原料,写出该原料在生产中的一种用途___________ 。

已知:相关金属离子c(Mn+)=0.1 mol·L-1生成氢氧化物沉淀的pH如下表所示:
| Fe2+ | Fe3+ | Al3+ | Zn2+ | |
| 开始沉淀 | 6.5 | 2.7 | 3.4 | 6.5 |
| 沉淀完全 | 9.7 | 3.7 | 4.7 | 8.5 |
(1)ZnFe2O4可写出ZnO·Fe2O3,则ZnFe2O4与H2SO4反应的化学方程式
(2)“氧化”步骤中发生的离子方程式为
(3)滤渣B的主要成分为
(4)“沉锌”反应中,往滤液加入NH4HCO3溶液,生成ZnCO3·Zn(OH)2及CO2,写出相应的离子方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


