解答题-工业流程题 适中0.65 引用1 组卷47
硒是人体不可缺少的微量元素,硒的应用范围非常广泛。以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)提取硒一种工艺流程如下:
等)提取硒一种工艺流程如下:
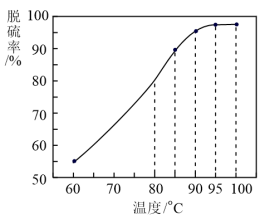
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;_______ ,最佳脱硫温度为_______ 。 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可采用硫脲 联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
联合亚硫酸钠进行“控电位还原”,下表是“氧化酸浸”液中主要粒子的电位。
控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原 ,该过程的还原反应(半反应)式为
,该过程的还原反应(半反应)式为_______ ,为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_______ V以上。
(4)“精制”过程中 先将Se浸出转化成硒代硫酸钠(
先将Se浸出转化成硒代硫酸钠( ),
), 再被
再被 酸化生成硒的离子方程式为
酸化生成硒的离子方程式为_______ 。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg⋅g ,则精硒中铁的质量分数为
,则精硒中铁的质量分数为_______ %。
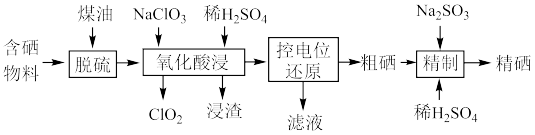
(1)“脱硫”时,脱硫率随温度的变化如图所示,试分析随温度的升高,脱硫率呈上升趋势的原因;
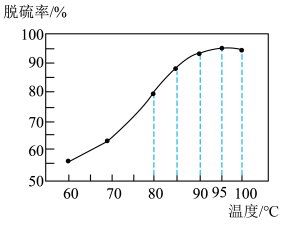
(3)“控电位还原”,是将电位高的物质先还原,电位低的物质保留在溶液中,以达到物质的分离。可采用硫脲
名称 |
|
|
|
|
| |
中位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
(4)“精制”过程中
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg⋅g
2024·安徽安庆·三模
类题推荐
随着人们对硒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)提取硒,设计流程如下:______ 。最佳温度是________ 。
(2)“氧化酸浸”中,Se转化成H2SeO3,该反应的离子方程式为_____________ 。
(3)采用硫脲[(NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
①控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原ClO2。该过程的还原反应(半反应)式为___________ 。
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_____ V。
(4)粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
①净化后的溶液中c(S2-)达到0.026 mol·L-1,此时溶液中的c(Cu2+)的最大值为________ ,精硒中基本不含铜。[Ksp(CuS)=1.3×10-36]
②硒代硫酸钠酸化生成硒的化学方程式为____________ 。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg·g-1,则精硒中铁的质量分数为________ %,与粗硒中铁含量为0.89%相比,铁含量明显降低。
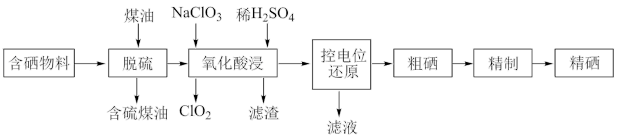

(2)“氧化酸浸”中,Se转化成H2SeO3,该反应的离子方程式为
(3)采用硫脲[(NH2)2CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
| 名称 | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Fe3+/Fe2+ | ClO2/Cl- | H2SeO3/Se |
| 电位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在
(4)粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)]→Na2S净化→H2SO4酸化等步骤。
①净化后的溶液中c(S2-)达到0.026 mol·L-1,此时溶液中的c(Cu2+)的最大值为
②硒代硫酸钠酸化生成硒的化学方程式为
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg·g-1,则精硒中铁的质量分数为
随着人们对硒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、 、
、 、
、 、
、 等)提取硒,设计流程如下:
等)提取硒,设计流程如下:
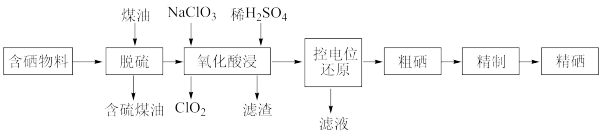
回答下列问题:
(1)“脱硫”时,测得脱硫率随温度的变化如上(如图)。随着温度的升高,脱硫率呈上升趋势,其原因是_____ 。最佳温度是_____ 。
(2)“氧化酸浸”中, 转化成
转化成 ,该反应的离子方程式为
,该反应的离子方程式为_____ 。
(3)采用硫[ ]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒子的电位。
①控制电位在 范围内,在氧化酸浸液中添加硫,可选择性还原ClO2。该过程的还原反应(半反应)式为
范围内,在氧化酸浸液中添加硫,可选择性还原ClO2。该过程的还原反应(半反应)式为_____ 。
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_____ V。
(4)粗硒的精制过程: 浸 出[Se转化成硒代硫酸钠(
浸 出[Se转化成硒代硫酸钠( )]
)] 净化
净化 酸化等步骤。
酸化等步骤。
①净化后的溶液中 达到
达到 ,此时溶液中的
,此时溶液中的 的最大值为
的最大值为_____ 。精硒中基本不含铜[ ]
]
②硒代硫酸钠酸化生成硒的化学方程式为_____ 。


回答下列问题:
(1)“脱硫”时,测得脱硫率随温度的变化如上(如图)。随着温度的升高,脱硫率呈上升趋势,其原因是
(2)“氧化酸浸”中,
(3)采用硫[
| 名称 | ||||||
| 电位/ |
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在
(4)粗硒的精制过程:
①净化后的溶液中
②硒代硫酸钠酸化生成硒的化学方程式为
随着人们对硒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学小组以含硒物料(主要含S、Se、Fe2O3、CuO、ZnO、SiO2等)为原料提取硒,设计的流程如图:
(1)“脱硫”时,测得脱硫率随温度的变化如图,最佳温度是____ 。____ ,该反应的离子方程式为____ 。
(3)采用催化剂联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。如表是“氧化酸浸”液中主要粒子的电位。
①控制电位在0.740-1.511V范围内,在氧化酸浸液中添加催化剂,可选择性还原ClO2,该过程的还原反应(半反应)式为____ 。
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在____ V以上。
(4)粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)])→Na2S净化→H2SO4酸化等。
①净化后的溶液中c(Na2S)达到0.026mol·L-1,此时溶液中的c(Cu2+)的最大值为____ mol·L-1,精硒中基本不含铜。([Ksp(CuS)=1.3×10-36])
②硒代硫酸钠酸化生成硒的离子方程式为_____ 。
(5)H2SeO4在水溶液中的电离方程式如下:H2SeO4=H++HSeO ,HSeO
,HSeO
 H++SeO
H++SeO 。已知0.01mol·L-1H2SeO4溶液的pH为x,则K(HSeO
。已知0.01mol·L-1H2SeO4溶液的pH为x,则K(HSeO )=
)=____ (写出含x的表达式)。

(1)“脱硫”时,测得脱硫率随温度的变化如图,最佳温度是

(3)采用催化剂联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位低的物质保留在溶液中,以达到硒与杂质金属的分离。如表是“氧化酸浸”液中主要粒子的电位。
| 名称 | Cu2+/Cu | Zn2+/Zn | Fe2+/Fe | Fe3+/Fe2+ | ClO2/Cl- | H2SeO3/Se |
| 电位/V | 0.345 | -0.760 | -0.440 | 0.770 | 1.511 | 0.740 |
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在
(4)粗硒的精制过程:Na2SO3浸出[Se转化成硒代硫酸钠(Na2SeSO3)])→Na2S净化→H2SO4酸化等。
①净化后的溶液中c(Na2S)达到0.026mol·L-1,此时溶液中的c(Cu2+)的最大值为
②硒代硫酸钠酸化生成硒的离子方程式为
(5)H2SeO4在水溶液中的电离方程式如下:H2SeO4=H++HSeO
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


