解答题-工业流程题 适中0.65 引用2 组卷87
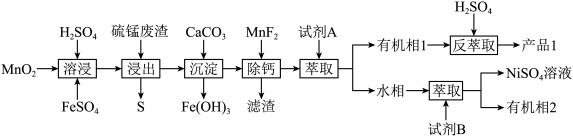
硫锰废渣的主要成分是MnS,还含有NiS、CoS以及少量铁的化合物,利用常压酸浸—溶剂萃取法从硫锰废渣中回收有价金属锰、钻、镍的工艺流程如下: 与
与 均稍过量;②溶液中离子浓度小于
均稍过量;②溶液中离子浓度小于 为沉淀完全;③
为沉淀完全;③ ;④
;④ 开始沉淀的
开始沉淀的 分别为7.2、7.7、8.1。
分别为7.2、7.7、8.1。
回答下列问题:
(1)“溶浸”中发生反应的还原产物是_______ (填化学式)。MnS溶于 会生成
会生成 ,但本工艺“浸出”过程中无
,但本工艺“浸出”过程中无 产生,利用离子方程式说明原因
产生,利用离子方程式说明原因_______ 。
(2)“沉淀”中调节溶液 为3.5,此时
为3.5,此时
_______ 。
(3)“滤渣”中主要有 和
和_______ ,不能通过调节溶液的 完成“除钙”的原因是
完成“除钙”的原因是_______ 。
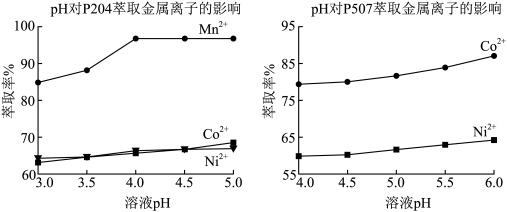
(4) 对萃取剂P204和P507萃取金属离子的影响如下图所示。据此推测,“产品1”中主要的金属阳离子是
对萃取剂P204和P507萃取金属离子的影响如下图所示。据此推测,“产品1”中主要的金属阳离子是_______ ,试剂B应选用_______ (填“P204”或“P507”)。 介质中,用
介质中,用 氧化
氧化 可沉淀出能用作镍镉电池正极材料的
可沉淀出能用作镍镉电池正极材料的 。写出该反应的离子方程式
。写出该反应的离子方程式_______ 。
回答下列问题:
(1)“溶浸”中发生反应的还原产物是
(2)“沉淀”中调节溶液
(3)“滤渣”中主要有
(4)
2024·四川绵阳·三模
类题推荐
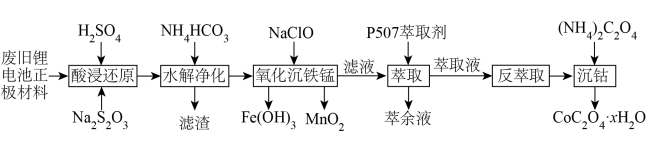
近年来,废旧锂离子电池的回收成为目前新能源产业重要的发展方向。某锂离子二次电池的正极材料主要为 ,还含有少量Al、Fe、Mn、Ni的化合物。通过如图流程利用废旧锂离子电池制备草酸钴晶体(
,还含有少量Al、Fe、Mn、Ni的化合物。通过如图流程利用废旧锂离子电池制备草酸钴晶体( ):
):
已知该工艺条件下,有关金属离子沉淀完全( )的pH见表:
)的pH见表:
回答下列问题:
(1)“酸浸还原”时, 发生的反应中氧化产物为硫酸盐的化学方程式为
发生的反应中氧化产物为硫酸盐的化学方程式为_______ 。
(2)水解净化的“滤渣”成分_______ 。
(3)氧化过滤的目的是沉铁和沉锰,其操作为控制体系的pH在4~5,加入NaClO溶液。写出其中沉铁的离子方程式_______ ;实际生产中,随着反应时间的延长,锰和铁的沉淀率逐渐增大,但钴的损失量也随之增大,可能的原因为:_______ 。
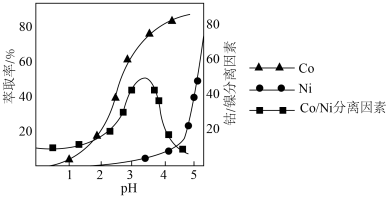
(4)利用“P507萃取剂”从“滤液”中分离 。萃取时,Co、Ni的浸出率和钴/镍分离因素与水相pH的如图所示。Co/Ni分离因素越大,表明萃取剂对Co/Ni分离效果越好。由图可知,萃取时的最佳水相pH为_______(填字母)。
。萃取时,Co、Ni的浸出率和钴/镍分离因素与水相pH的如图所示。Co/Ni分离因素越大,表明萃取剂对Co/Ni分离效果越好。由图可知,萃取时的最佳水相pH为_______(填字母)。

已知该工艺条件下,有关金属离子沉淀完全(
| 离子 | ||||||
| pH | 9.3 | 3.2 | 9.0 | 4.7 | 10.1 | 8.9 |
(1)“酸浸还原”时,
(2)水解净化的“滤渣”成分
(3)氧化过滤的目的是沉铁和沉锰,其操作为控制体系的pH在4~5,加入NaClO溶液。写出其中沉铁的离子方程式
(4)利用“P507萃取剂”从“滤液”中分离

| A.2.5 | B.3.0 | C.3.5 | D.4.0 |
硫锰净化废渣中Mn、Co和Ni主要以硫化物形式存在,还含有少量SiO2,采用如图工艺流程回收废渣中锰、钴、镍。

①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
②P204、P507为有机萃取剂。
回答下列问题:
(1)硫锰净化废渣预先粉碎的目的是_______ 。
(2)“除杂1”溶液的pH范围应调节为_______ ~6之间,“滤渣1”的主要成分是_______ 。
(3)“除杂2”中加入MnF2的目的是使Ca2+转化为CaF2沉淀除去,若溶液的pH偏低,将会导致Ca2+沉淀不完全,其原因是_______  。
。
(4)在NaOH溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,且转移1 mol电子时,放出热量为 。写出该反应的热化学方程式
。写出该反应的热化学方程式_______ 。
(5)“操作IV”的具体实验操作有_______ 、过滤、洗涤、干燥得到CoSO4•nH2O样品,采用热重分析法测定该样品中所含结晶水数,将样品加热到95℃时失掉1个结晶水,失重6.4%。则该CoSO4•nH2O样品的化学式为_______ 。

①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Mn2+ | Co2+ | Ni2+ |
| 开始沉淀pH | 6.3 | 1.5 | 8.1 | 7.1 | 6.9 |
| 完全沉淀pH | 8.3 | 2.8 | 10.1 | 9.15 | 8.9 |
回答下列问题:
(1)硫锰净化废渣预先粉碎的目的是
(2)“除杂1”溶液的pH范围应调节为
(3)“除杂2”中加入MnF2的目的是使Ca2+转化为CaF2沉淀除去,若溶液的pH偏低,将会导致Ca2+沉淀不完全,其原因是
(4)在NaOH溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH,且转移1 mol电子时,放出热量为
(5)“操作IV”的具体实验操作有
硫锰净化废渣中Mn、Co和Ni主要以硫化物形式存在,还含有少量SiO2,采用如图工艺流程回收废渣中锰、钴、镍。

①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
②P204、P507为有机萃取剂。
回答下列问题:
(1)硫锰净化废渣预先粉碎的目的是___ 。
(2)“除杂1”溶液的pH范围应调节为___ ~6之间,“滤渣1”的主要成分是___ 。
(3)“除杂2”中加入MnF2的目的是使Ca2+转化为CaF2沉淀除去,若溶液的pH偏低,将会导致Ca2+沉淀不完全,其原因是__ [Ksp(CaF2)=5.3×10-9,Ka(HF)=6.3×10-4]。
(4)NiSO4在NaOH溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的化学方程式___ 。
(5)“操作IV”的具体实验操作有___ 、过滤、洗涤、干燥得到CoSO4·nH2O样品,采用热重分析法测定该样品中所含结晶水数,将样品加热到95℃时失掉1个结晶水,失重6.4%。则该CoSO4·nH2O样品的化学式为___ 。

①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe2+ | Fe3+ | Mn2+ | Co2+ | Ni2+ |
| 开始沉淀pH | 6.3 | 1.5 | 8.1 | 7.1 | 6.9 |
| 完全沉淀pH | 8.3 | 2.8 | 10.1 | 9.15 | 8.9 |
②P204、P507为有机萃取剂。
回答下列问题:
(1)硫锰净化废渣预先粉碎的目的是
(2)“除杂1”溶液的pH范围应调节为
(3)“除杂2”中加入MnF2的目的是使Ca2+转化为CaF2沉淀除去,若溶液的pH偏低,将会导致Ca2+沉淀不完全,其原因是
(4)NiSO4在NaOH溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的化学方程式
(5)“操作IV”的具体实验操作有
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


