解答题-工业流程题 适中0.65 引用3 组卷266
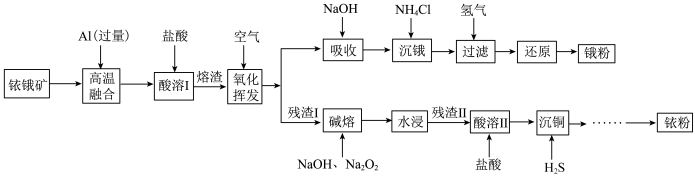
铱(77Ir)和锇(76Os)属于铂族金属,与金、银合称贵重金属,可以用于电气、精密仪表、催化剂等领域。铱锇矿的主要成分有Ir、Os、Ir2O3、OsO2,还含有CuO和SiO2等杂质,从铱锇矿中提取铱和锇的流程如下:
回答下列问题:
(1)“酸溶I”的目的是___________ ;酸溶I后溶渣的主要成分除Ir、Os外,还有___________ (填化学式)。
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为___________ 。
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应 ,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是
,生成的锇盐要立即过滤,滤饼要经无水乙醇多次洗涤,用无水乙醇洗涤的优点是___________ 。
(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为___________ 。
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中
___________ mol/L。[已知:25℃,H2S溶于水形成饱和溶液时, ;H2S的电离常数
;H2S的电离常数 ,
, ;
; ]
]
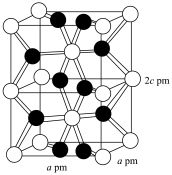
(6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为 ,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为
,设NA为阿伏加德罗常数的值,则IrO2的摩尔质量为___________ (用代数式表示)g/mol。
回答下列问题:
(1)“酸溶I”的目的是
(2)“氧化挥发”是将溶渣置于300~800℃的管式炉内,通入空气氧化。再用NaOH溶液吸收OsO4生成Na2OsO4,该反应的离子方程式为
(3)“沉锇”时,NH4Cl与Na2OsO4发生反应
(4)“碱熔”时,“残渣I”中的Ir与Na2O2反应生成IrO2·nNa2O和O2,该反应的化学方程式为
(5)“沉铜”过程中,当通入H2S达到饱和时测得溶液的pH=1,此时溶液中
(6)化合物 IrO2的四方晶格结构如图所示,其棱边夹角均为90°。已知IrO2晶体密度为
2024·辽宁·三模
类题推荐
利用软锰矿(主要成分是MnO2,还含少量CaO、MgO、SiO2、Al2O3等杂质)制取高纯硫酸锰的工艺流程如图所示。

已知:常温下,一些金属氢氧化物沉淀的pH如表:
常温下,一些难溶电解质的溶度积常数如表:
回答下列问题:
(1)滤渣1的主要成分是_______ (填化学式);将软锰矿、铁屑和硫酸按一定比例放入反应装置中,搅拌、加热反应一定时间,其中搅拌、加热的目的是_______ ;从“深度除杂”后的溶液中得到MnSO4固体的操作为_______ 、降温结晶、过滤、洗涤和干燥。
(2)“浸取”时,溶液中的Fe2+与MnO2反应生成Fe3+的离子方程式为_______ ,“浸出液”需要鼓入一段时间空气后,再进行“沉铁”的原因是_______ 。
(3)“沉铁、铝”时,加CaCO3控制溶液pH范围是_______ ;常温下,Ksp[Al(OH)3]=________ 。
(4)“深度除杂”中加入MnF2可以除去_______ 离子和_______ 离子,原因是_______ 。

已知:常温下,一些金属氢氧化物沉淀的pH如表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Al(OH)3 |
| 开始沉淀pH | 1.5 | 6.5 | 7.7 | 3.8 |
| 沉淀完全pH | 3.7 | 9.7 | 9.8 | 5.2 |
| 难溶电解质 | MnF2 | CaF2 | MgF2 |
| Ksp | 5.3×10-3 | 1.5×10-10 | 7.4×10-11 |
(1)滤渣1的主要成分是
(2)“浸取”时,溶液中的Fe2+与MnO2反应生成Fe3+的离子方程式为
(3)“沉铁、铝”时,加CaCO3控制溶液pH范围是
(4)“深度除杂”中加入MnF2可以除去
氮化镓(GaN)具有优异的光电性能。一种利用炼锌矿渣[主要含铁酸镓Ga2(Fe2O4)2、铁酸锌ZnFe2O4、SiO2]制备GaN的工艺流程如下:
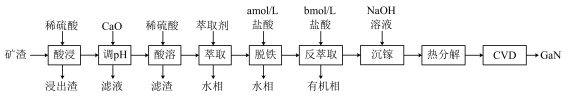
已知:
①Ga与Al同主族,化学性质相似。
②常温下, ,
, ,
, 。
。
③ 、
、 在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
在该工艺条件下的反萃取率(进入水相中金属离子的百分数)与盐酸浓度的关系见下表。
回答下列问题:
(1)“酸浸”时 发生反应的离子方程式为
发生反应的离子方程式为___________ 。“酸溶”所得滤渣的主要成分是___________ (填化学式)。
(2)“酸浸”所得浸出液中 、
、 浓度分别为0.003mol/L和1mol/L。常温下,为尽可能多地提取
浓度分别为0.003mol/L和1mol/L。常温下,为尽可能多地提取 并确保不混入
并确保不混入 ,“调pH”时需用CaO调pH略小于
,“调pH”时需用CaO调pH略小于___________ (假设调pH时溶液体积不变)。
(3)“反萃取”时,所用盐酸的浓度
___________ (选填上表中盐酸的浓度)。
(4)“沉镓”时,若加入NaOH的量过多,会导致 的沉淀率降低,原因是
的沉淀率降低,原因是___________ (用离子方程式表示)。
(5)利用CVD(化学气相沉积)技术,将热分解得到的 与
与 在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为
在高温下反应可制得GaN,同时生成另一种产物,该反应化学方程式为___________ 。
(6)①GaN的熔点为1700℃, 的熔点为77.9℃,则
的熔点为77.9℃,则 晶体类型为
晶体类型为___________ 。
②GaN晶体的一种立方晶胞如图所示。该晶体密度为 ,GaN的式量为Mr,则晶胞边长为
,GaN的式量为Mr,则晶胞边长为___________ nm。(列出计算式, 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)


已知:
①Ga与Al同主族,化学性质相似。
②常温下,
③
| 盐酸浓度/ | 反萃取率/% | |
| 2 | 86.9 | 9.4 |
| 4 | 69.1 | 52.1 |
| 6 | 17.5 | 71.3 |
(1)“酸浸”时
(2)“酸浸”所得浸出液中
(3)“反萃取”时,所用盐酸的浓度
(4)“沉镓”时,若加入NaOH的量过多,会导致
(5)利用CVD(化学气相沉积)技术,将热分解得到的
(6)①GaN的熔点为1700℃,
②GaN晶体的一种立方晶胞如图所示。该晶体密度为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网