解答题-工业流程题 适中0.65 引用1 组卷92
新型锂电池正极材料 有望取代广泛使用的
有望取代广泛使用的 ,由软锰矿(主要成分为
,由软锰矿(主要成分为 ,还含有少量
,还含有少量 、FeO、
、FeO、 、
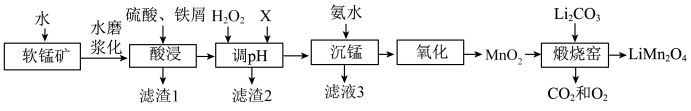
、 等杂质)为原料制备锰酸锂的流程如图:
等杂质)为原料制备锰酸锂的流程如图: ,
, ;
;
②离子浓度 mol⋅L-1时除尽;
mol⋅L-1时除尽;
回答下列问题:
(1)软锰矿水磨浆化处理的作用是___________ 。
(2)锂电池放电时正极反应式为 ,则锰酸锂中锰元素的化合价为
,则锰酸锂中锰元素的化合价为___________ 。
(3)用 代替
代替 氧化除杂,反应物利用率会更高,理由是
氧化除杂,反应物利用率会更高,理由是___________ 。
(4)调pH时加入的X不能选用下列物质的是______。
(5)常温下,调节 ,除去
,除去 、
、 ,写出
,写出 已经除尽的计算过程:
已经除尽的计算过程:___________ 。
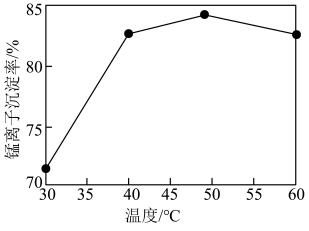
(6)其他条件一定,沉锰过程中 的沉淀率与溶液温度的关系如下图。:50℃后,随溶液温度升高,
的沉淀率与溶液温度的关系如下图。:50℃后,随溶液温度升高, 的沉淀率下降的原因是
的沉淀率下降的原因是___________ 。 反应的化学方程式为
反应的化学方程式为___________ 。
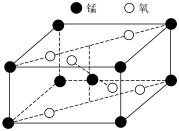
(8)一种锰的氧化物四方晶胞结构如图所示,该晶胞由 和
和 构成。
构成。___________ ,基态 的价层电子轨道表示式为
的价层电子轨道表示式为___________ 。
②离子浓度
回答下列问题:
(1)软锰矿水磨浆化处理的作用是
(2)锂电池放电时正极反应式为
(3)用
(4)调pH时加入的X不能选用下列物质的是______。
| A.NaOH | B.氨水 | C. | D. |
(5)常温下,调节
(6)其他条件一定,沉锰过程中
(8)一种锰的氧化物四方晶胞结构如图所示,该晶胞由
2024·江西·二模
类题推荐
新型锂电池正极材料锰酸锂(LiMn2O4)有望取代广泛使用的LiCoO2。工业上用某软锰矿(主要成分为MnO2,还含有少量铁、铝及硅等氧化物)为原料制备锰酸锂的流程如图:
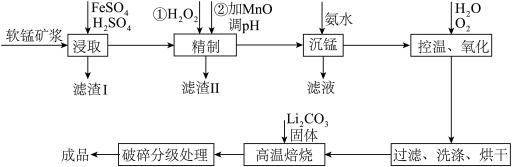
已知: lg2=0.3, =8,25℃有关物质的溶度积常数:
=8,25℃有关物质的溶度积常数:
(1)已知锂电池放电时正极的电极反应式为:LiMn2O4+e-+Li+ ===Li2Mn2O4,则锰酸锂中锰元素的化合价为____ 。
(2)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为_____ ,检验还含有Fe2+的方法是______ 。
(3)“精制”中加入H2O2的量比理论值大的多,其主要原因是______ ,若所得溶液中锰离子的浓度为1 mol·L-1,则加入氧化锰调节pH的范围为____ (当溶液中离子浓度小于10-5 mol·L-1时可以认为沉淀完全)。
(4)“沉锰”得到的是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为Mn3O4,若控温氧化时溶液的pH随时间的变化如下图,则15~150 min内滤饼中一定参加反应的成分是______ ;判断的理由是____ (用化学方程式表示)。

(5)写出高温煅烧生成锰酸锂的化学方程式_______ 。

已知: lg2=0.3,
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 8.0×10-16 | 4.0×l0-38 | 5.12×10-33 | 4.0×l0-14 |
(2)“浸取”得到的浸取液中阳离子主要是Mn2+,生成Mn2+的离子方程式为
(3)“精制”中加入H2O2的量比理论值大的多,其主要原因是
(4)“沉锰”得到的是Mn(OH)2和Mn2(OH)2SO4滤饼,二者均可被氧化为Mn3O4,若控温氧化时溶液的pH随时间的变化如下图,则15~150 min内滤饼中一定参加反应的成分是

(5)写出高温煅烧生成锰酸锂的化学方程式
LiMn2O4是一种锂离子电池的正极材料。用高锰酸钾废渣(主要成分为MnO2、Fe2O3、Al2O3、SiO2)和硫铁矿(主要成分为FeS2)制备LiMn2O4的工艺流程如图:
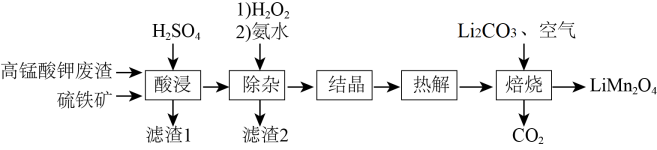
已知:①酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属间离子;
②25℃时,相关物质的Ksp见表。
(1)酸浸。MnO2与FeS2反应生成Fe3+和SO 的离子方程式为
的离子方程式为____ 。保持温度、浸取时间不变,能提高锰元素浸出率的措施有____ 。
(2)除杂。欲使溶液中的Al3+、Fe3+沉淀完全,调节溶液的pH最小值为____ (当溶液中某离子浓度c≤1×10-5mol·L-1时,可认为该离子沉淀完全)。
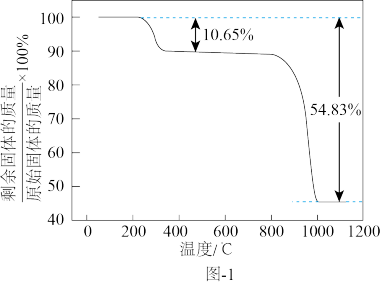
(3)热解。在真空中加热分解MnSO4•H2O,测得固体的质量随温度变化如图1所示。真空热解MnSO4•H2O制备Mn3O4,需控制的温度为_____ 。(写出计算推理过程)。
(4)焙烧。生成LiMn2O4的反应中,还原剂是____ (填化学式)。
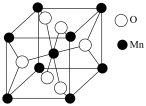
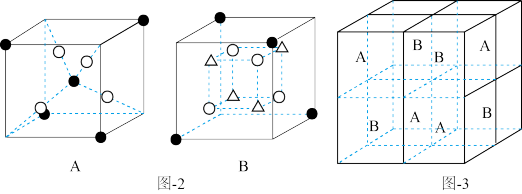
(5)一种LiMn2O4晶胞可看成由图2中A、B单元按图3方式构成。图2中“○”表示O2-,则“●”表示的微粒是____ (填离子符号)。

已知:①酸浸液主要含有Mn2+、Fe2+、Fe3+、Al3+等金属间离子;
②25℃时,相关物质的Ksp见表。
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
(2)除杂。欲使溶液中的Al3+、Fe3+沉淀完全,调节溶液的pH最小值为
(3)热解。在真空中加热分解MnSO4•H2O,测得固体的质量随温度变化如图1所示。真空热解MnSO4•H2O制备Mn3O4,需控制的温度为

(4)焙烧。生成LiMn2O4的反应中,还原剂是
(5)一种LiMn2O4晶胞可看成由图2中A、B单元按图3方式构成。图2中“○”表示O2-,则“●”表示的微粒是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网