解答题-原理综合题 较难0.4 引用1 组卷68
近两年来,碳中和连续成为两会期间最受关注的议题之一, 的回收和利用对于改善环境,实现绿色发展至关重要。
的回收和利用对于改善环境,实现绿色发展至关重要。
(1) 甲烷化反应最早由化学家PaulSabatier提出。已知:
甲烷化反应最早由化学家PaulSabatier提出。已知:
反应Ⅰ.
反应Ⅱ.
① 的结构式为
的结构式为_______ 。
② 甲烷化反应是
甲烷化反应是_______ (填“吸热”或“放热”)反应。
③反应Ⅰ的 和
和 为速率常数,与温度、催化剂有关)。若平衡后升高温度,则
为速率常数,与温度、催化剂有关)。若平衡后升高温度,则
_______ (填“增大”、“不变”或“减小”)。
(2)一定条件下, 与
与 反应可合成乙烯:
反应可合成乙烯: 。该反应分两步进行:
。该反应分两步进行:
ⅰ.
ⅱ.
 ,压强恒定为
,压强恒定为 时,将
时,将 的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示。
的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示。
 的平衡转化率为
的平衡转化率为_______ ,反应ⅰ的平衡常数
_______ ( 是以分压表示的平衡常数,分压
是以分压表示的平衡常数,分压 总压
总压 物质的量分数)。
物质的量分数)。
(3)一种以 和甲醇为原料,利用
和甲醇为原料,利用 和
和 纳米片
纳米片 作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。 为
为_______ 极,电解过程中阴极的电极反应式为_______ 。
②设 为阿伏加德罗常数的值,当电路中转移
为阿伏加德罗常数的值,当电路中转移 电子时,装置中生成
电子时,装置中生成 和
和 的数目共为
的数目共为_______ 。
(1)
反应Ⅰ.
反应Ⅱ.
①
②
③反应Ⅰ的
(2)一定条件下,
ⅰ.
ⅱ.
| 组分 | |||
| 物质的量分数 |
(3)一种以
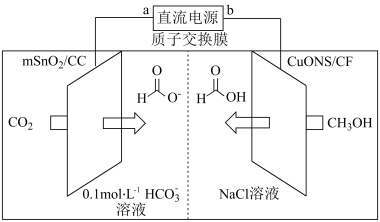
②设
2024·湖北·三模
类题推荐  资源化在推进能源绿色转型,实现“碳达峰、碳中和”中具有重要意义。
资源化在推进能源绿色转型,实现“碳达峰、碳中和”中具有重要意义。
Ⅰ. 与
与 催化重整制合成气是研究热点之一、发生的主要反应有:
催化重整制合成气是研究热点之一、发生的主要反应有:
反应①:
反应②:
(1)有关化学键键能数据如表:
则反应②的反应热
_______  。
。
(2)对于上述反位体系,下列说法错误的是_______ 。
A.增大 的浓度,反应①②的正反应速率均增加
的浓度,反应①②的正反应速率均增加
B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,可提高 的平衡转化率
的平衡转化率
(3)恒压下进行 与
与 催化重整实验。初始压强为
催化重整实验。初始压强为 ,起始投料
,起始投料 ,
, 和
和 的平衡转化率随温度变化曲线如图所示。
的平衡转化率随温度变化曲线如图所示。
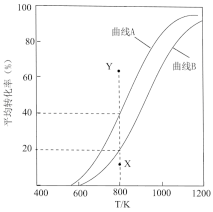
①曲线_______ (填“A”或“B”)表示 的平衡转化率。
的平衡转化率。
②800K,反应至 转化率达到X点时,v(正)
转化率达到X点时,v(正)_______ v(逆)(填“>”、“<”或“=”)。若要使 的转化率由X点达到Y点,改变的外界条件可以是
的转化率由X点达到Y点,改变的外界条件可以是_______ (答一条即可)。
③800K,反应①的分压平衡常数
_______ (分压=总压×物质的量分数)。
Ⅱ.利用电化学装置可实现 和
和 两种分子的耦合转化,其原理如图所示。
两种分子的耦合转化,其原理如图所示。
(4)阴极的电极反应式为_______ 。  催化重整对温室气体的减排具有重要意义,其反应为:
催化重整对温室气体的减排具有重要意义,其反应为: 。回答下列问题:
。回答下列问题:
(1)已知相关物质的燃烧热(
 ):
):
则 催化重整反应的
催化重整反应的
_______  。
。
(2)将原料按初始组成
 充入密闭容器中,保持体系压强为
充入密闭容器中,保持体系压强为
 发生反应。达到平衡时,
发生反应。达到平衡时,
 体积分数与温度的关系如图所示。
体积分数与温度的关系如图所示。
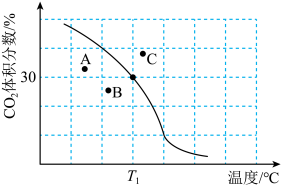
① 下,n(平衡时气体):n(初始气体)=
下,n(平衡时气体):n(初始气体)=_______ 。该温度下,此反应的平衡常数
_______  (以分压表示,分压=总压强×气体成分的物质的量分数。保留1位小数)。
(以分压表示,分压=总压强×气体成分的物质的量分数。保留1位小数)。
②若A、B、C三点表示不同温度和压强下达到平衡时 的体积分数,则
的体积分数,则_______ 点对应的平衡常数最小,理由是_______ 。
(3)其他条件相同,在不同催化剂(A、B)作用下,反应
 进行相同时间后,
进行相同时间后,
 的产率随反应温度的变化如图所示。
的产率随反应温度的变化如图所示。

①在催化剂A、B作用下,它们正、逆反应活化能差值分别用 表示,则
表示,则
_______  (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。
②y点对应的
_______ z点对应的 。
。
(4) 和
和
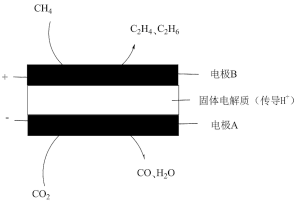
 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
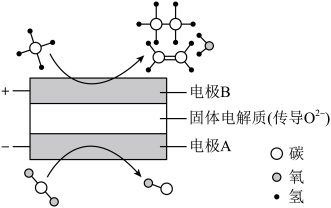
①阴极的电极反应式为_______ 。
②若生成的乙烯和乙烷的体积比为 ,则消耗的
,则消耗的 和
和 的体积比为
的体积比为_______ 。  的化学转化利用路径有效推动了
的化学转化利用路径有效推动了 高附加值利用和化工行业绿色低碳负碳化进程。回答下列问题。
高附加值利用和化工行业绿色低碳负碳化进程。回答下列问题。
Ⅰ.利用 合成淀粉的研究成果已经被我国科学家发表在《Nature》杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在《Nature》杂志上。其涉及的关键反应如下:
①
②
③
(1)反应①在________ (选填“高温”“低温”或“任何温度”)下自发进行,反应③中
________ 。
(2)在一定条件下,向某体积恒为 的容器中按
的容器中按 的比例通入气体,只发生反应③,下列情况可以说明反应③已经达到平衡的是________。
的比例通入气体,只发生反应③,下列情况可以说明反应③已经达到平衡的是________。
(3)在催化剂作用下,按 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持总压强为
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持总压强为 ,测得不同温度下,反应达到平衡后
,测得不同温度下,反应达到平衡后 的转化率、
的转化率、 的选择性如图所示:
的选择性如图所示:
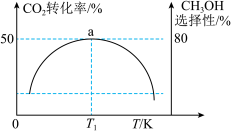
已知: 的选择性
的选择性 。
。
在 时,若反应从开始到达到
时,若反应从开始到达到 点所用时间为
点所用时间为 ,则这
,则这 内
内
________  ,反应②的
,反应②的
________ 。(可用分数表示。 指用平衡分压代替平衡浓度进行计算的平衡常数,
指用平衡分压代替平衡浓度进行计算的平衡常数, 的平衡分压
的平衡分压 的物质的量分数
的物质的量分数 )
)
Ⅱ.近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示。
的回收利用,其工作原理如图所示。
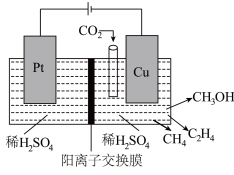
(4)请写出 电极上产生
电极上产生 的电极反应式:
的电极反应式:_________ 。
(5)在一定条件下,该装置 电极附近制得的
电极附近制得的 、
、 、
、 的物质的量之比为
的物质的量之比为 ,则当Pt电极附近有
,则当Pt电极附近有 气体产生时(已折算为标准状况,不考虑水蒸气,忽略气体的溶解),制得的甲醇的质量为
气体产生时(已折算为标准状况,不考虑水蒸气,忽略气体的溶解),制得的甲醇的质量为_________ 。
Ⅰ.
反应①:
反应②:
(1)有关化学键键能数据如表:
| 化学键 | H-O | C=O | ||
| 键能/ | 436 | 463 | 803 | 1076 |
(2)对于上述反位体系,下列说法错误的是
A.增大
B.恒容密闭容器中当气体密度不变时,反应达到平衡状态
C.加入催化剂,可提高
(3)恒压下进行

①曲线
②800K,反应至
③800K,反应①的分压平衡常数
Ⅱ.利用电化学装置可实现

(4)阴极的电极反应式为
(1)已知相关物质的燃烧热(
| 物质 | |||
| 燃烧热 |
(2)将原料按初始组成

①
②若A、B、C三点表示不同温度和压强下达到平衡时
(3)其他条件相同,在不同催化剂(A、B)作用下,反应

①在催化剂A、B作用下,它们正、逆反应活化能差值分别用
②y点对应的
(4)

①阴极的电极反应式为
②若生成的乙烯和乙烷的体积比为
Ⅰ.利用
①
②
③
(1)反应①在
(2)在一定条件下,向某体积恒为
| A.混合气体密度不再改变 |
| B.混合气体平均相对分子质量不再改变 |
| C.容器中 |
| D. |
(3)在催化剂作用下,按

已知:
在
Ⅱ.近年来,有研究人员用

(4)请写出
(5)在一定条件下,该装置
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


